Opis przypadku | Case report
Zastosowanie terapii podciśnieniowej z płukaniem roztworem podchlorynu o stężeniu 800 ppm w leczeniu zakażenia miejsca operowanego i zaburzeń gojenia powłok brzusznych u pacjentki z chorobą Leśniowskiego-Crohna o ciężkim przebiegu
The use of negative-pressure therapy with instillation of 800 ppm hypochlorite solution in the management of surgical site infection and abdominal wall defects in a patient with severe Leśniowski-Crohn’s disease
Maciej Borejsza-Wysocki1, Pamela Jeske1, Bartosz Grzechulski1, Adam Bobkiewicz 1, Michał Molin2, Tomasz Banasiewicz
1, Michał Molin2, Tomasz Banasiewicz  1
1
1 Klinika Chirurgii Ogólnej, Endokrynologicznej i Onkologii Gastroenterologicznej, Uniwersytet Medyczny w Poznaniu
2 Oddział Chirurgii Onkologicznej, Szpital Specjalistyczny im Jędrzeja Śniadeckiego w Nowym Sączu
Adres do korespondencji: Maciej Borejsza-Wysocki, Klinika Chirurgii Ogólnej, Endokrynologicznej i Onkologii Gastroenterologicznej. Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu, ul. Przybyszewskiego 49, 60-355 Poznań, e-mail: maciejbw@gmail.com
Nadesłano: 2.05.2023
Zaakceptowano: 15.05.2023
Opublikowano: 7.07.2023
LECZENIE RAN 2023; 20 (2): 70–76
Streszczenie
Choroba Leśniowskiego-Crohna jest czynnikiem ryzyka występowania zakażenia miejsca operowanego. W pracy przedstawiono przypadek 62-letniej pacjentki z powikłaną chorobą Leśniowskiego-Crohna. Z powodu ostrego rzutu choroby, miejscowego zaawansowania choroby, obecności przetok i ropni okołostomijnych, a także przepukliny okołostomijnej u pacjentki wystąpiło głębokie zakażenie miejsca operowanego, wymagające trzykrotnej reoperacji. W przypadku licznych, dużych ran obejmujących znaczną powierzchnię powłok brzusznych z obecnością stomii zastosowanie terapii podciśnieniowej z płukaniem pozwala na optymalizację procesu leczenia i gojenia rany. Odseparowanie skażonego środowiska stomii od łożysk ran wydaje się kluczowym elementem powodzenia leczenia. Odpowiedni dobór płynu płuczącego umożliwia intensyfikację leczenia zakażenia w pierwszej fazie wystąpienia zakażenia miejsca operowanego oraz sprzyja dalszemu postępowi gojenia ran.
Słowa kluczowe: choroba Leśniowskiego-Crohna, terapia podciśnieniowa, terapia podciśnieniowa z płukaniem, powikłania, zakażenie miejsca operowanego.
Abstract
Leśniowski-Crohn’s disease is a risk factor for surgical site infection. We present a case of a 62-year-old patient with complicated Leśniowski-Crohn’s disease. Due to the acute phase of the disease, local advancement of the inflammatory process, the presence of peristomal fistulas and abscesses, as well as parastomal hernia, the patient developed a deep surgical site infection, requiring three re-operations. In the case of numerous, large wounds covering a large area of the abdominal wall with the presence of a stoma, the use of negative-pressure therapy with instillation allows for the optimization of the wound treatment and healing process. Separating the stoma as a source of contaminated content from the wound bed is a key element in the success of treatment. Appropriate selection of the instilled fluid enables the intensification of the treatment in the first phase of infection of surgical site infection and promotes further progress of wound healing.
Key words: Leśniowski-Crohn’s disease, negative pressure wound therapy, negative pressure wound therapy with instillation, complications, surgical site infection.
Wprowadzenie
Choroba Leśniowskiego-Crohna wymaga często interwencji chirurgicznej. W tej grupie chorych operacje obarczone są dużym ryzykiem powikłań ze względu na biologię choroby, stosowane leczenie, stan ogólny chorych i często liczne wcześniejsze zabiegi chirurgiczne [1]. Zaleca się jak najlepsze przygotowanie pacjentów w celu redukcji ryzyka wystąpienia powikłań [2]. Prehabilitacja, czyli kompleksowe przygotowanie pacjentów, powinna być stałym elementem strategii chirurgicznej [3]. Oczywiście, nawet kompleksowe przygotowanie przedoperacyjne nie jest w stanie wyeliminować całkowicie ryzyka wystąpienia powikłań.
Wprowadzenie podciśnieniowej terapii ran (negative presurre wound therapy – NPWT) do codziennej praktyki chirurgicznej zrewolucjonizowało strategię leczenia ran. Jedną z modyfikacji i uzupełnień tej metody jest jej połączenie z jednoczesnym podawaniem płynu, czyli terapia podciśnieniowa z płukaniem (negative pressure wound therapy with instillation – NPWTi) [4]. Płyn może być podawany przez ten sam port, przez który prowadzona jest terapia podciśnieniowa (podaż płynu odbywa się przy wyłączonej opcji ssania, forma taka nazywana jest namaczaniem), lub przez osobno założony na opatrunek port, co powoduje przepływ płynu pomiędzy portem podającym a odbierającym. Zastosowanie płukania może zmniejszać obciążenie bakteryjne rany, skracać czas gojenia, poprawiać środowisko rany, pobudzając migrację fibroblastów, ziarninowanie czy naskórkowanie [5]. Użycie standardowej NPWT w ranach powikłanych gęstą wydzieliną ropną, z dużą ilością martwicy rozpływnej czy dodatkowym skażeniem rany, np. stolcem wydostającym się ze stomii lub przetoki, może być niewystarczające. W takich przypadkach płukanie może zwiększać efektywność NPWT. Ponadto wydzielina z rany głębokiej o nieregularnych kształtach gromadzi się często w ranie i jej kieszeniach, co zaburza naturalne mechanizmy gojenia się rany. Terapia podciśnieniowa z płukaniem przeciwdrobnoustrojowym rozpuszcza i wypłukuje resztki komórkowe, martwiczą tkankę, bakterie oraz produkty ich rozpadu, w tym cytokiny zapalne czy metaloproteinazy [6].
Płukanie może stanowić również element zwiększający efektywność eliminacji i usuwania biofilmu. Rodzaj płynu płuczącego wynika z charakteru rany, stopnia jej czystości, ryzyka zakażenia i jej lokalizacji. Przy doborze odpowiedniego płynu powinno się z jednej strony brać pod uwagę efekt antyseptyczny i antybakteryjny, z drugiej bezpieczeństwo i jak najmniejszy negatywny wpływ na tkanki [7]. Wśród wielu możliwych opcji jedną z zalecanych, zależnie od szczegółowych wskazań, są podchloryny. Istotne jest ich bezpieczeństwo w przypadku kontaktu z jamami ciała, szczególnie jamą otrzewnową. Zastosowany przez autorów niniejszej pracy płyn to elektrochemicznie aktywowany wodny roztwór soli zawierający wodę, kwas podchlorawy (podchloryn sodu: > 0,08%) służący do oczyszczania, nawilżania, odkażania i zapobiegania infekcjom w ranach ostrych i przewlekłych. Zawiera on podchloryn sodu i kwas podchlorawy w stężeniu 0,08%, co odpowiada 800 ppm. Wytwarza wilgotne środowisko w ranie, umożliwiając właściwy proces gojenia. Preparat może być używany do oczyszczania, dezynfekcji i płukania ran ostrych, przewlekłych i zainfekowanych oraz do odkażania oparzeń pierwszego i drugiego stopnia.
Opis przypadku
Pacjentka, lat 62, została przyjęta do kliniki w trybie planowym z powodu objawów przewlekłej podniedrożności przewodu pokarmowego spowodowanej zaostrzeniem choroby podstawowej (choroba Leśniowskiego-Crohna) końcowego odcinka jelita grubego (w obrębie stomii) oraz tkanek okołostomijnych, z aktywnymi przetokami jelitowo-skórnymi oraz dużą przepukliną okołostomijną (ryc. 1).
W wywiadzie wieloletnie leczenie zachowawcze, w tym terapia biologiczna (bez zadowalającej odpowiedzi klinicznej) oraz steroidoterapia, kontynuowana do momentu przeprowadzenia zabiegu (stopniowe zmniejszanie dawki glikokortykosteroidów), cukrzyca insulinozależna od 6 lat, nadciśnienie tętnicze. W przeszłości chora była pięciokrotnie operowana – wykonano odcinkowe resekcje jelita grubego, stan po wyłonieniu kolostomii końcowej.
Pacjentka została zakwalifikowana do zabiegu chirurgicznego ze względu na nasilające się zaburzenia drożności przewodu pokarmowego, w tym epizody niedrożności wymagające interwencji w trybie ostrodyżurowym z powodu krytycznego zwężenia stomii. Skóra w okolicy kolostomii zmieniona pozapalnie, przetoki jelitowo-skórne w okolicy stomii oraz ropnie podskórne. Chorą poinformowano o znacząco podwyższonym ryzyku wystąpienia powikłań pooperacyjnych, w tym zaburzeń gojenia i zakażeniu miejsca operowanego.
I etap leczenia
Rodzaj zabiegu: laparotomia z dostępu wokół stomii. Wycięcie końcowego odcinka jelita grubego wraz ze stomią i przetokami okołostomijnymi. Ze względu na masywne, lite zrosty wewnątrzbrzuszne oraz stan pacjentki zdecydowano, by nie wykonywać dodatkowego cięcia środkowego i wyłonić stomię w górnym biegunie rany.
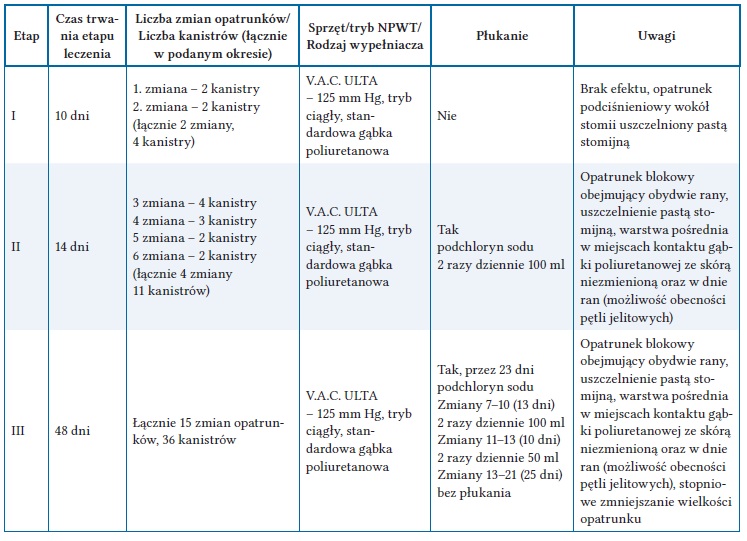
Postępowanie pooperacyjne: antybiotykoprofilaktyka, a nastepnie antybiotykoterapia empiryczna, leczenie miejscowe, terapia podciśnieniowa (tab. I).
Tabela I. Charakterystyka etapów leczenia za pomocą terapii podciśnieniowej
Przebieg pooperacyjny: zakażenie miejsca operowanego, zaburzenie gojenia rany z jej rozejściem. Trudności w zaopatrzeniu stomii. Rehabilitacja ruchowa. Żywienie doustne oraz częściowe żywienie pozajelitowe. Z uwagi na brak postępu gojenia oraz cechy głębokiego zakażenia miejsca operowanego zdecydowano o reoperacji w 10. dobie
po zabiegu.
II etap leczenia
Rozpoznanie: stan po operacji jak wyżej. Rozejście rany. Zakażenie miejsca operowanego. Dysfunkcja i zapadnięcie stomii.
Rodzaj zabiegu: laparotomia z dostępu pośrodkowego z wycięciem starej blizny. Uwolnienie licznych zrostów. Przełożenie kolostomii końcowej z lewego nadbrzusza do prawego podbrzusza. Pierwotne zamknięcie rany.
Postępowanie pooperacyjne: kontynuacja antybiotykoterapii (zmiana antybiotyku zgodnie z posiewem), terapia podciśnieniowa w miejscu po wcześniejszej lokalizacji stomii z płukaniem, terapia podciśnieniowa rany laparotomijnej z płukaniem. Szczegółowe dane dotyczące stosowanej terapii podciśnieniowej przedstawiono w tabeli I.
Przebieg pooperacyjny: rozejście rany w miejscu po stomii, rozejście rany po laparotomii, głębokie zakażenie miejsca operowanego. Brak wgajania stomii, powierzchowna martwica stomii, zapadnięcie stomii ze stopniowym poszerzaniem się rany okołostomijnej. Rehabilitacja ruchowa. Żywienie doustne oraz częściowe żywienie pozajelitowe. Decyzję o reoperacji podjęto po 14 dniach.
III etap leczenia
Rozpoznanie: stan po operacjach jak wyżej. Dysfunkcja i zapadnięcie przemieszczonej stomii. Rozejście rany po laparotomii z jej zakażeniem. Rozejście rany po uprzednio zlikwidowanej stomii.
Rodzaj zabiegu: cięcie pośrodkowe z dostępu poprzedniego (cięcie pośrodkowe). Przełożenie stomii z podbrzusza prawego do nadbrzusza prawego. Zbliżenie brzegów ran i szwy odroczone ran po uprzednio wyłonionych stomiach i rany laparotomijnej (ryc. 2).
Postępowanie pooperacyjne: kontynuacja antybiotykoterapii do 5. dnia po zabiegu (spadek parametrów zapalnych i brak klinicznych cech zakażenia miejscowego), terapia podciśnieniowa ran z płukaniem po wcześniejszych lokalizacjach stomii (lewe nadbrzusze oraz prawe podbrzusze; ryc. 3). Szczegółowe dane dotyczące stosowanej terapii podciśnieniowej przedstawiono w tabeli I.
Przebieg pooperacyjny: bardzo powolne gojenie przez ziarninowanie. Utrzymanie terapii podciśnieniowej na ranach po laparotomii i zlikwidowanych bądź przeniesionych stomiach. Sytuacyjne zbliżanie brzegów ran w celu zmniejszenia ich powierzchni i głębokości (ryc. 4–7). Rehabilitacja ruchowa. Żywienie doustne oraz częściowe żywienie pozajelitowe. Pacjentkę wypisano do domu w 48. dobie hospitalizacji.
Omówienie
Na podstawie retrospektywnych analiz wykazano, że występowanie chorób zapalnych jelit jest niezależnym czynnikiem powikłań gojenia ran oraz występowaniem zakażenia miejsca operowanego [8]. Co więcej, bardzo często pacjenci z chorobą Leśniowskiego-Crohna wymagają podjęcia leczenia operacyjnego, pozostając na leczeniu biologicznym lub steroidoterapii (zabiegi pilne lub przyspieszone) a także w ostrej fazie choroby, co dodatkowo zaburza naturalne mechanizmy gojenia ran [9].
Wprowadzenie NPWT do leczenia ran zrewolucjonizowało strategię ich leczenia. W grupach ryzyka wystąpienia zakażenia miejsca operowanego zaleca się stosowanie profilaktycznej NPWT [10, 11]. W sytuacjach klinicznych z pooperacyjnymi dużymi ubytkami tkankowymi przedniej ściany jamy brzusznej, obecnością zakażenia miejsca operowanego, a przede wszystkim bliskości stomii stosowanie NPWT nie tylko pozwala na uzyskanie postępu gojenia, lecz także na zaopatrzenie ran i stomii bez ryzyka kontaminacji ran treścią jelitową.
Zachowanie ciągłości stosowania NPWTi pozwala na skuteczną minimalizację miejscowego stanu zapalnego. Terapia podciśnieniowa z płukaniem może także stanowić terapię pomostową w zaawansowanej fazie zakażenia miejscowego. W miarę postępu gojenia, minimalizacji treści ropnej lub zmniejszenia wydzielania przez ranę, a także przy obserwowanej poprawie miejscowej tkanek NPWTi można zastąpić standardową NPWT (minimalizacja kosztów). Ważny pozostaje także fakt pozytywnego wpływu grupy cytokin na profil gojenia, co przy przedłużonej
NPWTi może wiązać się z „wypłukiwaniem” cytokin o działaniu stymulującym gojenie.
Autorzy niniejszej pracy wprowadzili NPWTi jako metodę z wyboru. Z doświadczenia autorów wynika, że zastosowanie NWPTi w ranach powikłanych może stanowić ważną alternatywę dla standardowego postępowania. Ponadto NPWTi jest akceptowaną metodą poprawiającą skuteczność standardowej terapii NPWT i może być pomocna w skomplikowanych sytuacjach klinicznych, takich jak leczenie metodą otwartego brzucha czy w leczeniu zakażonych implantów [6].
W przypadku NPWTi bardzo ważna jest decyzja o rodzaju stosowanego płynu. Nie ma aktualnych zaleceń wskazujących jeden standardowy roztwór przeciwdrobnoustrojowy, który należałoby stosować w NPWTi. W praktyce używa się bardzo wielu płynów: od 0,9-procentowego roztworu soli fizjologicznej do szerokiej gamy środków antyseptycznych. Wybór stosowanego płynu płuczącego uzależnia się od:
- spodziewanego efektu (zmniejszenie gęstości wydzieliny, eliminacja mechaniczna, działanie przeciwbakteryjne, biofilm w ranie),
- bezpieczeństwa stosowania w przypadku ran penetrujących lub mających kontakt z jamami ciała.
Wybrany przez autorów płyn o stężeniu > 0,08% podchlorynu sodu i kwasu podchlorawego ma, wg charakterystyki produktu, szerokie spektrum działania przeciwdrobnoustrojowego (bakterie Gram-dodatnie i Gram-ujemne, grzyby, przetrwalniki, wirusy), bardzo dobrą tolerancję tkankową potwierdzoną w teście HET-CAM i może być stosowany do ran mających kontakt z jamą otrzewnową. Te właściwości, łączące efekt przeciwdrobnoustrojowy z bezpieczeństwem stosowania, zdecydowały
o jego wyborze.
Kolejnym problemem klinicznym była wielkość, nieregularny kształt i rozmieszczenie ran na całej niemal powierzchni przedniej ściany jamy brzusznej. Implikowało to dwa istotne elementy postępowania: ochronę skóry zdrowej oraz ochronę pętli jelitowych mogących znajdować się potencjalnie w dnie ran, tuż pod tkanką ziarninującą.
Bezpośredni kontakt gąbki poliuretanowej ze skórą nieuszkodzoną oraz pętlami jelitowymi jest przeciwwskazany ze względu na potencjalne ryzyko uszkodzenia skóry i jelit podczas terapii i zmiany opatrunku (co może prowadzić do powstawania przetok). Aby uniknąć tych powikłań, autorzy zastosowali warstwę kontaktową – specjalny nieprzylepny opatrunek siatkowy umieszczany pomiędzy gąbką poliuretanową a łożyskiem rany. Metoda ta była bezpieczna i powszechnie akceptowana jako modyfikacja standardowego leczenia NPWT. Inną opcją możliwą do zastosowania w tego rodzaju sytuacjach jest gąbka z polialkoholu winylowego (PVA), która charakteryzuje się mniejszą tendencją do przerastania ziarniną zapalną. Niestety, w prezentowanym przypadku ropna wydzielina była zbyt gęsta, aby można było zastosować wypełniacz PVA (małe oka wypełniacza PVA w kontraście do wypełniacza poliuretanowego).
Wnioski
Choroba Leśniowskiego-Crohna jest czynnikiem ryzyka występowania zakażenia miejsca operowanego.
W pracy przedstawiono przypadek 62-letniej pacjentki z powikłana chorobą Leśniowskiego-Crohna. Z powodu ostrego rzutu choroby, miejscowego zaawansowania choroby, obecności przetok i ropni okołostomijnych, a także przepukliny okołostomijnej u pacjentki wystąpiło głębokie zakażenie miejsca operowanego, wymagające trzykrotnej reoperacji. W przypadku licznych, dużych ran obejmujących znaczną powierzchnię powłok brzusznych z obecnością stomii zastosowanie terapii podciśnieniowej z płukaniem pozwala na optymalizację procesu leczenia i gojenia rany. Odseparowanie skażonego środowiska stomii od łożysk ran wydaje się kluczowym elementem powodzenia leczenia. Odpowiedni dobór płynu płuczącego umożliwia intensyfikację leczenia zakażenia w pierwszej fazie wystąpienia zakażenia miejsca operowanego oraz sprzyja dalszemu postępowi gojenia ran.
Oświadczenie
Tomasz Banasiewicz jest konsultantem: KCI Acelity, Hartmann, Smith and Nephew, Convatec, Molnlycke.
Adam Bobkiewicz jest konsultantem Hartmann.
Pozostali autorzy deklarują brak konfliktu interesów.
Piśmiennictwo
- Lahes S, Fischer C, Spiliotis AE i wsp. Effect of immunosuppressive medication on postoperative complications following abdominal surgery in Crohn’s disease patients. Int J Colorectal Dis 2022; 37: 2535–2542. DOI: 10.1007/s00384-022-04287-4.
- Patel KV, Darakhshan AA, Griffin N i wsp. Patient optimization for surgery relating to Crohn’s disease. Nat Rev Gastroenterol Hepatol 2016; 13: 707–719. DOI: 10.1038/nrgastro.2016.158.
- Jeske P, Wojtera B, Banasiewicz T. Prehabilitation – current role in surgery. Pol Przegl Chir 2022; 94: 64–72. DOI: 10.5604/01.3001.0015.7340.
- Bobkiewicz A, Studniarek A, Krokowicz L i wsp. Instillation-TIME (iTIME) as a rationale amendment for TIME conception. Is there enough evidence for the efficiency of negative pressure wound therapy with instillation (iNPWT) to announce a breakthrough idea for wound treatment? Negative Pressure Wound Therapy Journal 2019; 6: 7–8. DOI: https://doi.org/10.18487/npwtj.v6i2.50
- Aycart MA, Eble DJ, Ross KM, Orgill DP. Mechanisms of action of instillation and dwell negative pressure wound therapy with case reports of clinical applications. Cureus 2018; 10: e3377. DOI: 10.7759/cureus.3377.
- Kim PJ, Attinger CE, Constantine T i wsp. Negative pressure wound therapy with instillation: International consensus guidelines update. Int Wound J 2020; 17: 174–186. DOI: 10.1111/iwj.13254.
- Kramer A, Dissemond J, Kim S i wsp. Consensus on wound antisepsis: update 2018. Skin Pharmacol Physiol 2018; 31: 28–58. DOI: 10.1159/000481545.
- Uchino M, Ikeuchi H, Tsuchida T i wsp. Surgical site infection following surgery for inflammatory bowel disease in patients with clean-contaminated wounds. World J Surg 2009; 33: 1042–1048. doi: 10.1007/s00268-009-9934-4.
- Wang AS, Armstrong EJ, Armstrong AW. Corticosteroids and wound healing: clinical considerations in the perioperative period. Am J Surg 2013; 206: 410–407. DOI: 10.1016/j.amjsurg.2012.11.018.
- Shiroky J, Lillie E, Muaddi H i wsp. The impact of negative pressure wound therapy for closed surgical incisions on surgical site infection: A systematic review and meta-analysis. Surgery 2020 ; 167: 1001–1009. DOI: 10.1016/j.surg.2020.01.018.
- Borejsza-Wysocki M, Bobkiewicz A, Francuzik W i wsp. Effect of closed incision negative pressure wound therapy on incidence rate of surgical site infection after stoma reversal: a pilot study. Videosurgery Miniinv 2021; 16: 686–696. DOI: 10.5114/wiitm.2021.106426.

