Artykuł przeglądowy | Review paper
Rola banków tkanek w medycynie regeneracyjnej ze szczególnym uwzględnieniem przeszczepów
alogenicznej skóry ludzkiej
The role of tissue banks in regenerative medicine with
particular emphasis on allogenic human skin grafts
Anna Hepa-Banasik![]() 1, Magdalena Szatan
1, Magdalena Szatan![]() 1, Justyna Glik
1, Justyna Glik![]() 1,2, Anna Słaboń
1,2, Anna Słaboń![]() 1, Marcin Gierek
1, Marcin Gierek![]() 1, Karolina Ziółkowska
1, Karolina Ziółkowska![]() 1, Katarzyna Czerny
1, Katarzyna Czerny![]() 1, Artur Wielgórecki
1, Artur Wielgórecki![]() 1, Przemysław Strzelec
1, Przemysław Strzelec![]() 1, Agnieszka Klama-Baryła
1, Agnieszka Klama-Baryła![]() 1, Wojciech Łabuś
1, Wojciech Łabuś![]() 1
1
1 Centrum Leczenia Oparzeń im. dr. Stanisława Sakiela w Siemianowicach Śląskich, Polska
2 Zakład Organizacji Leczenia Ran Przewlekłych, Wydział Nauk o Zdrowiu w Katowicach, Śląski Uniwersytet Medyczny w Katowicach, Polska
Adres do korespondencji: Anna Hepa-Banasik, Centrum Leczenia Oparzeń im. dr. Stanisława Sakiela, ul. Jana Pawła II, 41-100 Siemianowice Śląskie, Polska, e-mail: hepa.anna@gmail.com
Nadesłano: 20.08.2023
Zaakceptowano: 15.09.2023
Opublikowano: 30.09.2023
LECZENIE RAN 2023; 20 (3): 103–113
DOI: 10.60075/lr.v20i3.47
Spis treści:
Streszczenie
Bank tkanek to wysoko wyspecjalizowane laboratorium, którego zadaniem jest pozyskiwanie, obróbka materiału biologicznego zgodnie z przyjętymi procedurami, przechowywanie oraz dystrybucja alogenicznych przeszczepów tkankowych do zakładów opieki zdrowotnej. Przeszczepy tkankowe znajdują swoje zastosowanie w takiej dziedzinie medycyny regeneracyjnej jak leczenie rozległych i głębokich ran oparzeniowych oraz przewlekłych. W niniejszym przeglądzie omówiono rolę banków tkanek w dostępie do alogenicznych przeszczepów skóry ludzkiej oraz problem zapotrzebowania i deficytu alogenicznej skóry ludzkiej w Polsce.
Słowa kluczowe: alogeniczne przeszczepy skóry ludzkiej, bank tkanek, rana przewlekła, rana oparzeniowa.
Abstract
A tissue bank is a highly specialized laboratory maintained to collect, prepare, store, and distribute certain allogenic tissue grafts to healthcare facilities. Tissue transplants are used in specific areas of regenerative medicine, including the treatment of extensive and deep burns and chronic wounds. This review discusses the role of tissue banks in the transplantation of allogenic human skin grafts and the problem of the deficit of allogenic human skin in Poland.
Key words: allogenic human skin grafts, tissue bank, chronic wound, burn wound.
Wstęp
Bankowanie tkanek i komórek stanowi dziedzinę medycyny transplantacyjnej. Zadaniem banku tkanek jest przygotowanie i przechowywanie, do czasu zastosowania klinicznego, przeszczepów tkanek i komórkowych produktów leczniczych pobranych od zmarłych lub żywych dawców. Przygotowane w bankach tkanek i komórek przeszczepy mogą znaleźć zastosowanie we wszystkich dostępnych specjalnościach zabiegowych, wspomagając lub wręcz umożliwiając leczenie chirurgiczne. Przeszczepy tkankowe i komórkowe produkty lecznicze wykorzystywane są w zabiegach rekonstrukcyjnych ubytków tkanek powstałych w wyniku urazu, zmian degeneracyjnych czy po rozległym wycięciu tkanek z powodu nowotworu oraz w leczeniu wad wrodzonych lub nabytych [1, 2]. W tym ujęciu na szczególną uwagę mogą zasługiwać rozlegle i głęboko oparzeni chorzy z deficytem zdrowej skóry do wykonania autologicznego przeszczepu. Alternatywą kliniczną w tej grupie chorych może być wykorzystanie biologicznych substytutów skóry, do których można zaliczyć alogeniczne przeszczepy skóry ludzkiej pobrane od dawcy zmarłego [3, 4].
Bank tkanek z definicji stanowi specjalistyczne laboratorium, którego zadaniem jest przygotowanie przeszczepów alogenicznych tkanek i komórkowych produktów leczniczych w celu przeszczepienia na potrzeby chirurgii rekonstrukcyjnej. Przygotowane z nich odpowiednie przeszczepy są przechowywane i w dalszym etapie udostępniane zakładom opieki zdrowotnej [5]. Umożliwia leczenie pacjentów z wykorzystaniem najnowszych i najskuteczniejszych terapii z zakresu transplantologii i medycyny regeneracyjnej. Bank spełnia wymagania Ustawy transplantacyjnej z dnia 1 lipca 2005 r. o pobieraniu, przechowywaniu i przeszczepianiu komórek, tkanek i narządów, w tym prowadzi niezbędną dokumentację dotyczącą przygotowania autologicznych komórkowych produktów leczniczych, jak również alogenicznych, biostatycznych i biowitalnych przeszczepów tkankowych. Posiada pomieszczenia i urządzenia spełniające warunki wymagane ustawowo, jak również odpowiednio wykwalifikowany personel. Ma on niezbędne do prowadzonej działalności pozwolenia Ministra Zdrowia na gromadzenie, przetwarzanie, przechowywanie i dystrybucję tkanek i komórek zgodę GIF na przygotowanie komórkowych produktów leczniczych terapii zaawansowanej ATMP.
Materiały i metody
Przeglądu literatury dokonano, posługując się słowami kluczowymi: „alogeniczne przeszczepy skóry ludzkiej”, „bank tkanek”, „bioinżynieria”, „donacja”. Przeszukano bazę PubMed. W toku analizy literatury usystematyzowano zebrany materiał dotyczący roli banków tkanek w przeszczepianiu alogenicznych przeszczepów skórnych i przedstawiono w niniejszym artykule.
Wyniki
Po wprowadzeniu słów kluczowych do bazy danych PubMed: allogenic skin grafts otrzymano 4675 rekordów. Następnie użyto takich filtrów, jak: publikacje z ostatnich 5 lat, ludzka skóra, anglojęzyczne publikacje, dzięki którym uzyskano docelowo 526 artykułów. Zdecydowana większość wyświetlonych pozycji nie dotyczyła bezpośrednio alogenicznej skóry ludzkiej, tylko traktowała o komórkach macierzystych bądź innych tematach zbliżonych, ale niedotyczących niniejszego przeglądu. W pracy finalnie zdecydowano się na wykorzystanie 45 z 526 pozycji.
Biomateriały
Zapotrzebowanie na materiały, które będą w stanie zastąpić zniszczone tkanki i narządy wciąż rośnie. Materiały te noszą nazwę biomateriałów, a związaną z nimi dyscyplinę nauki nazwano inżynierią biomateriałów. Biomateriały powinny charakteryzować się biozgodnością, bezpieczeństwem, efektywnością, brakiem toksyczności, brakiem immunogenności, biodegradowalnością lub funkcjonalną długotrwałością [6, 7]. Ze względu na pochodzenie materiału tkankowego, przeszczepy dzieli się na:
- ksenogeniczne – pozyskiwane od osobników obcego gatunku, wymagana jest tolerancja immunologiczna, występuje możliwość przeniesienia zwierzęcych wirusów;
- alogeniczne – w obrębie tego samego gatunku, dostępne bezpośrednio, ale wymagana jest tolerancja immunologiczna;
- autologiczne – gdy komórki pochodzą z tego samego ustroju, są immunologicznie akceptowane, ale nie są dostępne bezpośrednio [8].
Na rycinie 1 przedstawiono alogeniczny biostatyczny przeszczep skóry.
Do najkorzystniejszej z form zalicza się przeszczep autologiczny, czyli taki, w którym sam pacjent jest dla siebie dawcą. Na przykład przy wykorzystaniu skóry własnej, pobranej z miejsca nieuszkodzonego, a następnie przeszczepionej na ranę oparzeniową nie obserwuje się odpowiedzi układu immunologicznego [8, 9]. Ograniczenia związane ze stosowaniem autologicznych wolnych przeszczepów skóry pośredniej grubości (WPSPG) wymuszają poszukiwanie nowych metod i środków leczenia, np. u ciężko oparzonych pacjentów. Alternatywną procedurą ratującą życie w terapii rozległych oparzeń pełnej grubości skóry, w przypadku których występuje deficyt pól dawczych, jest wykonanie przeszczepu wyhodowanych in vitro autologicznych keratynocytów i fibroblastów będącymi produktami leczniczymi terapii zaawansowanej ATMP lub opracowanych na drodze inżynierii tkankowej naturalnych substytutów skóry (opatrunków biologicznych) [10–12]. W zależności od zastosowanych procedur przetwarzania tkanek po pobraniu oraz metod ich następczej konserwacji i przechowywania wyróżnia się:
- przeszczepy biowitalne – zawierają żywe komórki, np. przeszczepy rogówki poddane po pobraniu jedynie chłodzeniu w płynie odżywczym z antybiotykami oraz przeszczepy zastawek serca i naczyń krwionośnych poddane krioprezerwacji (kontrolowanemu zamrażaniu w obecności czynnika ochronnego);
- przeszczepy biostatyczne – pozbawione żywych komórek, do których zalicza się sterylizowane radiacyjne przeszczepy kości, chrząstki, skóry czy owodni [8].
Obiecującą alternatywą dla autologicznych przeszczepów skóry jest tzw. bezkomórkowa macierz skórna (acellular dermal matrix – ADM). Bezkomórkowa macierz skórna to tkanka przeszczepu alogenicznego, która jest odpowiednio przetwarzana w celu usunięcia wszystkich komórek naskórka i skóry, przy zachowaniu pozostałej bioaktywnej matrycy skórnej. Przykłady przedstawiono na rycinach 2 i 3.
W pracy zespołu Dai i wsp. przedstawiono podział substytutów skóry ze względu na budowę histologiczną. Wyróżniono naskórkowe, skórne i złożone substytuty skóry, w zależności od zawartego w nich składnika skóry. Następnie dokonano podziału na określone kategorie w zależności od ich składu i źródła materiału (np. naturalne i syntetyczne). Ponieważ nie ma idealnej opcji dla substytutów skóry, które spełniałyby wszystkie kryteria optymalnego gojenia się ran, trwają badania oceniające i rozwijające różne opcje substytutów skóry [13, 14].
W przypadku rozlegle i głęboko oparzonych pacjentów (z deficytem miejsc dawczych) można rozważyć podanie komórek skóry (keratynocytów i fibroblastów) hodowanych in vitro. Jedną z możliwych dróg podania wyhodowanych in vitro keratynocytów i/lub fibroblastów może być aerozol zawiesiny komórek w żelu bogatopłytkowo-leukocytarnym bezpośrednio na przygotowane miejsce biorcze (ranę oparzeniową) (ryc. 4A, B, 5). Do uzyskania wymaganej liczby hodowlanych autologicznych komórek skóry wymagane są około 3 tygodnie.
Istnieje również możliwość wykorzystania komórek alogenicznych. Komórki alogeniczne pochodzą od pacjentów, którzy mieli założoną hodowle in vitro autologicznych komórek skóry, jednak zmarli przed podaniem własnych, wyhodowanych komórek. W tej sytuacji istnieje możliwość wykorzystania tej hodowli dla innego pacjenta. Dlatego komórki alogeniczne są uważane za produkt gotowy do użycia [15].
Terapia ran przewlekłych również może odbywać się z wykorzystaniem materiału pochodzącego z banku tkanek. Do powstania rany przewlekłej może dojść na skutek przedłużającej się fazy zapalnej podczas procesu gojenia, co uniemożliwia wystąpienie kolejnych etapów regeneracji skóry. Typowe leczenie ran przewlekłych może obejmować stosowanie autoprzeszczepów oraz aloprzeszczepów pobranych od dawców zmarłych. Niemniej terapia rozległych lub głębokich ran może wymagać dodatkowo wdrożenia wybranych zaawansowanych form terapii obejmujących stosowanie m.in. produktów inżynierii tkankowej lub produktów leczniczych terapii zaawansowanej ATMP, np. mezenchymalnych komórek macierzystych w celu zmniejszenia stanu zapalnego i przyspieszenia procesu gojenia [16, 17].
Wraz z gwałtownie rosnącą liczbą chorych cierpiących z powodu cukrzycy typu 2 na świecie przewiduje się wzrost liczby przypadków przewlekłych, trudno gojących się lub niegojących się ran i owrzodzeń, tzw. stóp cukrzycowych. Pomimo stale podnoszonego poziomu wiedzy w zakresie patofizjologii powstawania owrzodzeń w przebiegu cukrzycy to pielęgnacja i skuteczne leczenie tego typu ran stanowi nadal poważne wyzwanie terapeutyczne. Podobny problem dotyka chorych z owrzodzeniami troficznymi podudzi. Przewlekła niewydolność żylna staje się chorobą cywilizacyjną XXI w. W tym ujęciu wzrasta zainteresowanie rozwojem nowych typów terapii i zastosowania nowoczesnych opatrunków biologicznych [18]. Banki tkanek starają się sprostać tym problemom, wspierając lekarzy w przygotowaniu osocza bogatopłytkowego (platelet rich plasma – PRP). Jest ono koncentratem o szczególnie dużym stężeniu płytek krwi (PLT) w ograniczonej objętości osocza. Zawiera czynniki wzrostu oraz bioaktywne białka regulujące różnicowanie komórek, modulowanie ich rozwoju oraz stymulowanie aktywności. Na rycinie 6 przedstawiono iniekcję preparatu PRP.
Skóra ludzka jako źródło materiału biologicznego dla inżynierii tkankowej
Skóra jest największym narządem człowieka. Masa skóry dorosłego mężczyzny wraz z tkanką podskórną może wynosić nawet 18–20 kg, natomiast jej powierzchnia może osiągać u dorosłego człowieka 1,7–2 m2. Grubość skóry wynosi 0,5–4 mm [19]. Skóra ludzka jest bogatym w kolagen źródłem biomateriałów wykorzystywanych w inżynierii tkankowej. Natomiast od wyprodukowanych substytutów skóry oczekuje się, aby miały cechy fizjologiczne i strukturalne naturalnej skóry [6]. Zdrowa skóra pełni szereg funkcji. Zapewnia np. barierę ochronną przed drobnoustrojami, utratą wody i uszkodzeniami spowodowanymi promieniowaniem ultrafioletowym, bierze udział w termoregulacji, odgrywa rolę narządu zmysłu (dotyk, ból itp.). W wyniku urazu może dojść do powstania zaburzeń strukturalnej i funkcjonalnej integralności skóry. Proces gojenia się rany jest złożony i zwykle wielofazowy. W wyniku zaburzeń procesu gojenia może dojść do powstania ran przewlekłych [20–22]. Skóra ma budowę warstwową. Składa się z naskórka, skóry właściwej i tkanki podskórnej. Naskórek jest zbudowany z 6–20 warstw komórek pochodzenia ektodermalnego. W zależności od narażenia na czynniki środowiskowe liczba warstw komórek jest zmienna, szczególnie w warstwie komórek zrogowaciałych [19]. Wyróżnia się następujące:
- warstwa podstawna – zawiera komórki macierzyste i keratynocyty, których wzrost umożliwia regenerację naskórka, oraz komórki Merkla i melanocyty;
- warstwa kolczysta – stanowi konstrukcję nadającą skórze wytrzymałość na bodźce mechaniczne;
- warstwa ziarnista – złożona z tonofibryli i 2–6 warstw wrzecionowatych komórek o spłaszczonych jądrach komórkowych;
- warstwa jasna – nie występuje we wszystkich okolicach naskórka, zwykle brak jej w naskórku skóry cienkiej;
- warstwa rogowa – będącą z punktu widzenia ochrony przed urazami chemicznymi czy mechanicznymi najważniejszą warstwą naskórka. Składa się ona ze spłaszczonych, pozbawionych jąder komórkowych korneocytów wypełnionych keratyną i naturalnym czynnikiem nawilżającym [19];
- błona podstawna – bezkomórkowa warstwa łącząca naskórek ze skóra właściwą;
- blaszka jasna;
- skóra właściwa – zbudowana z mocnej tkanki łącznej poprzetykanej naczyniami włosowatymi. Sieć elastycznych włókien kolagenowych, retikulinowych i sprężystych wypełniają również sploty naczyń chłonnych, zakończenia nerwowe, a także gruczoły potowe i łojowe;
- warstwa brodawkowata – zbudowana z tkanki łącznej włóknistej zawierającej oprócz włókien kolagenowych i sprężystych znaczną ilość włókien siateczkowych;
- warstwa siateczkowata – zbudowana z bardzo gęstej sieci włókien kolagenowych i retikulinowych.
- blaszka ciemna;
- blaszka siateczkowata.
Tkanka podskórna zasadniczo nie należy do skóry. Jest z nią jedynie ściśle związana czynnościowo i anatomicznie. Grubość tkanki podskórnej jest osobniczo zmienna [19, 23].
Banki tkanek na świecie
Zapotrzebowanie na przeszczepy narządów i tkanek gwałtownie wzrosło na całym świecie w ciągu ostatniej dekady ze względu na zwiększoną częstość występowania niewydolności ważnych narządów, rosnący sukces i większą poprawę wyników po przeszczepie. Jednak niedostępność odpowiednich narządów oraz tkanek do przeszczepów w celu zaspokojenia istniejącego zapotrzebowania doprowadziła do poważnych kryzysów związanych z niedoborem narządów i tkanek. W rezultacie nastąpił znaczny wzrost liczby pacjentów na listach oczekujących na przeszczep, a także liczby pacjentów umierających wpisanych na listę oczekujących. Ten kryzys związany z niedoborem narządów pozbawił tysiące pacjentów nowej, lepszej jakości życia i spowodował znaczny wzrost kosztów alternatywnej opieki medycznej, takiej jak dializy [24].
Polska
W Polsce powołano Krajowe Centrum Bankowania Tkanek i Komórek w Warszawie oraz Poltransplant, które są odpowiedzialne za koordynowanie procesem transplantacyjnym narządów oraz tkanek. Obowiązuje ustawa z 1 lipca 2005 r. o pobieraniu, przechowywaniu i przeszczepianiu komórek, tkanek i narządów (Dz. U. 2005 Nr 169, poz. 1411 z późn. zm.), rozporządzenie Ministra Zdrowia z 29 września 2016 r. w sprawie szczegółowych warunków pobierania, przechowywania i przeszczepiania komórek, tkanek i narządów (Dz.U. 2016 poz. 1674) oraz zarządzenie Ministra Zdrowia z 2 lipca 2010 r. w sprawie Centrum Organizacyjno-Koordynacyjnego ds. Transplantacji Poltransplant (Dz. Urz. MZ 2010 Nr 9 poz. 58 z późn. zm.). Dane dotyczące przeszczepiania narządów od zmarłych dawców w 2022 r. przedstawiono w tabeli I. W tabeli II zamieszczono informacje o liście oczekujących na przeszczep w 2022 r.
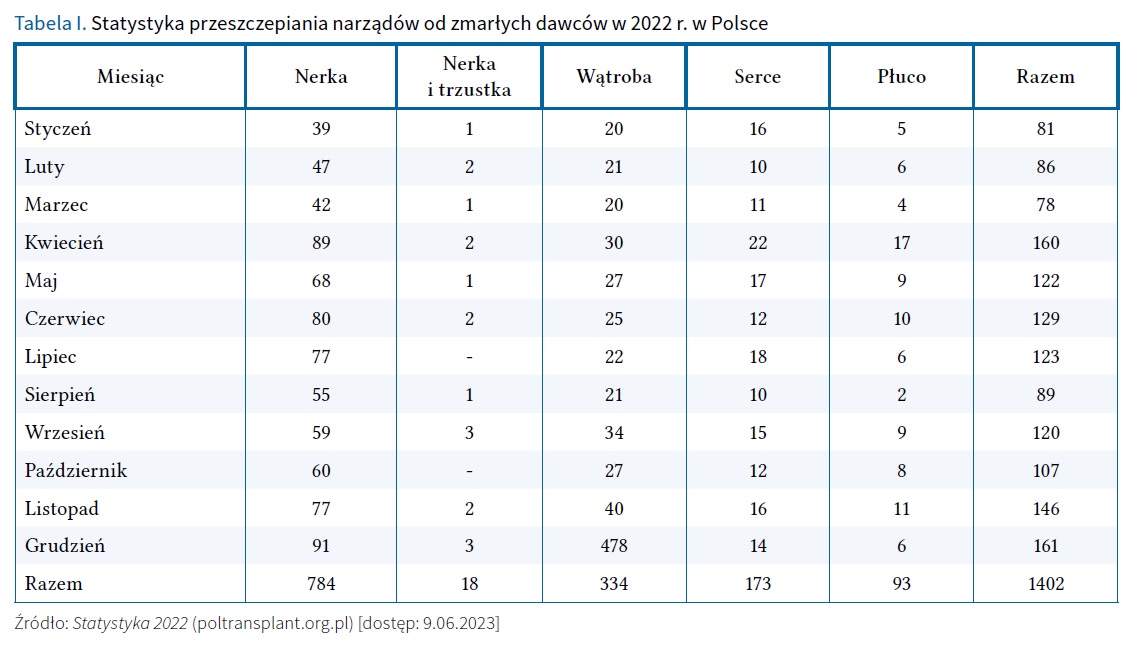
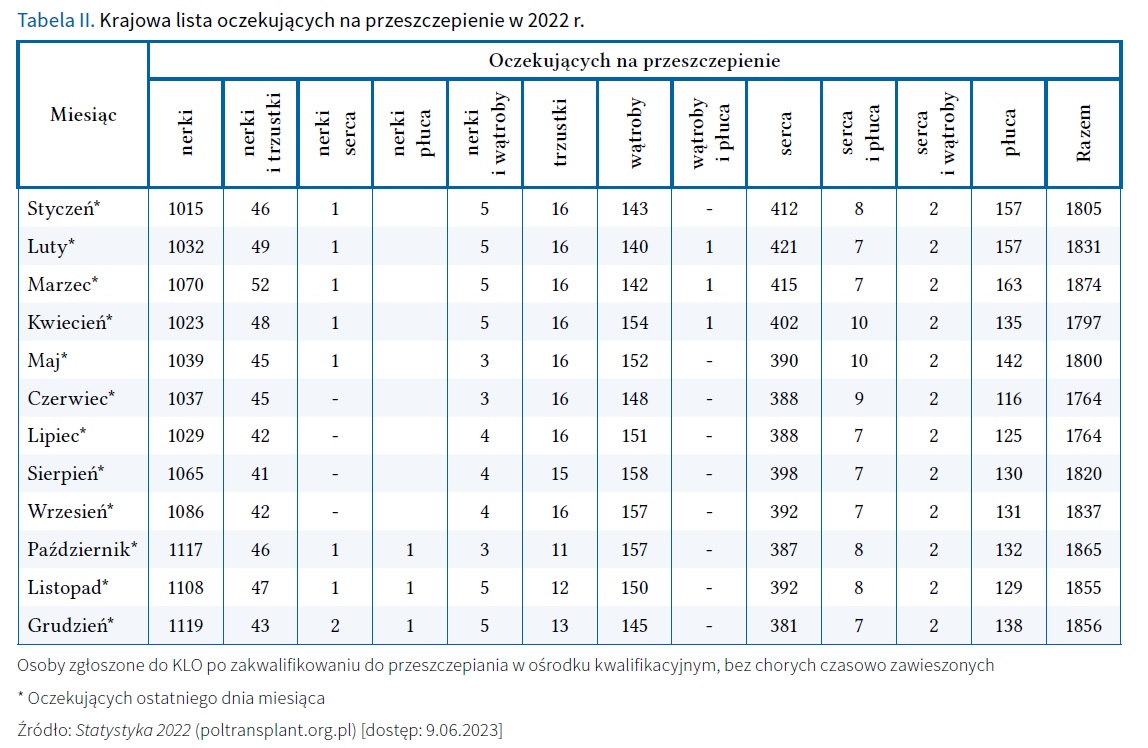
Na stronie Poltransplantu nie podano aktualnych danych dotyczących przeszczepiania skóry alogenicznej. Może to sugerować potrzebę uwzględniania danych dotyczących liczby pobrań oraz ilości pobranego materiału, jak również alokacji przygotowanych przeszczepów alogenicznej skóry.
Wielka Brytania
Dawstwo narządów tkanek po śmierci mózgu pozostaje preferowaną drogą dawstwa narządów zmarłego. W Wielkiej Brytanii obecny wskaźnik identyfikacji i kierowania potencjalnych dawców po śmierci mózgu wynosi 99%, natomiast wskaźnik testów określających zgon za pomocą kryteriów neurologicznych wynosi 86%. Zwiększenie dawstwa po stwierdzeniu śmierci mózgu będzie wymagało przede wszystkim dużego wzrostu obecnego wskaźnika zgody, wynoszącego 72%, do poziomu odpowiadającego wskaźnikowi zgody 80–90% osiąganemu w innych krajach europejskich [25, 26].
Azja
Działalność banków tkanek w regionach Azji i Pacyfiku jest regulowana przez dwie instytucje – Międzynarodową Agencję Energii Atomowej (MAEA) poprzez projekty Regionalnej Umowy o Współpracy, oraz przez Stowarzyszenie Bankowości Tkanek Chirurgicznych Azji i Pacyfiku (APASTB) [4, 27, 28].
Indie
W Indiach donacja również jest uregulowana prawnie, niemniej jednak znacząco różni się od przepisów prawa obowiązujących w Polsce. Poprawki do indyjskiej ustawy o transplantacji narządów ludzkich z 1994 r. ustanowiły legalność dawstwa tkanek i przeszczepów od zmarłych dawców oraz warunki, na jakich są one dozwolone. Znowelizowana ustawa, znana obecnie jako ustawa o transplantacji narządów i tkanek ludzkich z 1994 r., ma na celu zapobieganie komercjalizacji dawstwa tkanek i zagwarantowanie bezpieczeństwa miejscowych aloprzeszczepów. Rejestracja banków tkanek, zgodność z krajowymi standardami oraz powołanie koordynatorów transplantacji w szpitalach zarejestrowanych na podstawie ustawy są już obowiązkowe. Wprowadzono krajowy rejestr oraz regionalne i stanowe sieci dawstwa i przeszczepiania tkanek. Pomimo nowelizacji nadal istnieje kilka nieprawidłowości w podstawowej ustawie, ponieważ przeoczono niektóre różnice między dawstwem tkanek i narządów a przeszczepami. Obejmują one możliwość oddawania skóry w miejscach innych niż szpitale; oddawanie pozostałości tkanek medycznych i chirurgicznych, które nie stanowią żadnego zagrożenia dla żywego dawcy; brak wymogu zgodności między dawcą a biorcą; opóźnienie czasowe między dawstwem tkanki a przeszczepem, który uniemożliwia identyfikację biorcy w momencie dawstwa; łatwa dostępność alternatyw dla tkanek, co sprawia, że listy oczekujących są zbędne w przypadku wielu tkanek. Zasady wdrażania znowelizowanej ustawy zostały sformułowane w 2014 r., ale podobnie jak ustawa muszą zostać uchwalone przez państwowe zgromadzenia sanitarne, aby stały się powszechnie obowiązujące w kraju [29–31].
Chiny, Hongkong, Tajwan
Z różnych powodów osoby pochodzenia chińskiego (Chiny, Hongkong lub Tajwan) i południowoazjatyckiego (subkontynent indyjski), stanowiące dwie największe grupy mniejszości etnicznych w Ontario w Kanadzie, mogą być mniej skłonne do rejestracji w celu dawstwa narządów zmarłych niż ogół społeczeństwa, a ich rodziny mogą być mniej skłonne do wyrażenia zgody na dawstwo narządów w chwili śmierci. Aby potwierdzić tą hipotezę Alvin Ho-Ting Li wraz z zespołem przeprowadzili dwa badania populacyjne: (1) badanie przekrojowe rejestracji zmarłych dawców narządów od maja 2013 r. oraz (2) badanie kohortowe etapów postępowania w sprawie dawstwa narządów zmarłych u pacjentów, którzy zmarli w szpitalu od października 2008 r. do grudnia 2012 r. Wyniki badania wskazują, że w Ontario, w Kanadzie, Chińczycy i osoby pochodzenia południowoazjatyckiego rzadziej się rejestrują, a ich rodziny rzadziej wyrażają zgodę na dawstwo narządów w porównaniu z pozostałą opinią publiczną. Istnieje możliwość budowania wsparcia dla dawstwa narządów i tkanek w tych dwóch dużych społecznościach etnicznych w Kanadzie [28, 31].
Republika Południowej Afryki
Ma bardzo niskie i niezmienne wskaźniki dawstwa narządów. Kluczowym punktem na ścieżce dawstwa narządów jest uzyskanie świadomej zgody rodziny, która jest niezbędna przed rozpoczęciem dawstwa narządów. Nie opublikowano badań dotyczących wskaźnika zgody i czynników, które na to wpływają. Sześciu koordynatorów (3 z sektora państwowego i 3 z sektora prywatnego) zarejestrowało dane 83 kolejnych rodzin, do których zwrócono się w 16 szpitalach w okresie 1 roku. Zgoda na dawstwo narządów została udzielona dla 23 wniosków rodzinnych [n = 18 (sektor państwowy); n = 5 (sektor prywatny)]. Liczba rodzin, do których się zwrócono, była większa w sektorze państwowym (n = 74) niż w sektorze prywatnym (n = 9). Ogólny wskaźnik zgody wyniósł 27,7% [24,3% (sektor państwowy); 55,5% (sektor prywatny)]. Większość skierowań pochodziła z oddziałów urazowych i ratunkowych (n = 55; 66,3%), a bardzo niewiele z oddziałów intensywnej terapii (n = 25; 30,1%). Natychmiastowa resuscytacja płynowa była wymagana u 56 (67,5%) potencjalnych dawców. Większość rodzin (n = 74; 89,2%) była otwarta na prośbę o dawstwo narządów, niezależnie od ich ostatecznej decyzji dotyczącej dawstwa. Głównym powodem odmowy zgody było to, że było to sprzeczne z ich religią (n = 21) lub kulturą (n = 18) [32, 33]. Badanie to wykazało, że liczba rodzin, do których zwrócono się o zgodę na dawstwo narządów, była niska w Western Cape (niższa w sektorze prywatnym), przy niskim wskaźniku zgody (niższym w sektorze państwowym). Zarządzanie dawcami przez zespoły kliniczne musi być ciągłe i aktywne podczas procesu wyrażania zgody. Dyskusje na temat zgody (i inicjatywy uświadamiające społeczeństwo) muszą być wrażliwe na religijne i kulturowe zastrzeżenia dotyczące dawstwa narządów oraz radzić
sobie z nimi [34, 35].
Malezja
Luka między popytem a podażą narządów ludzkich do przeszczepów rośnie w Malezji, pomimo wysiłków rządów na rzecz promowania rejestracji dawców. Czynniki wpływające na gotowość do oddania krwi są kontekstowe i różnią się w zależności od kraju. Badania te koncentrują się głównie na wyborze najbardziej odpowiedniego systemu dawstwa narządów poprzez czynniki wpływające na chęć dawstwa w Malezji. Celem tego badania jest nadanie priorytetu czynnikom działającym jako filary systemu dawstwa narządów oraz wybór najbardziej odpowiedniego systemu dawstwa narządów dla Malezji [36].
Na podstawie wyników wielokryterialnej metody hierarchicznej analizy problemów decyzyjnych (analytical hierarchal process – AHP) oczywiste jest, że postrzeganie dawstwa (0,36) ma najwyższy priorytet w wpływaniu na wskaźniki dawstwa narządów, a następnie status społeczno-ekonomiczny (0,32), czynniki demograficzne (0,23) i zachęty finansowe (0,09). Ponadto uzyskane wyniki kwestionują istniejący system dobrowolnego oddawania krwi w Malezji i przedstawiają podejście domniemane jako odpowiedni system do zwiększenia wskaźnika dawstwa zmarłych w Malezji. Podejście domniemane promuje rolę pracowników służby zdrowia w uzyskiwaniu zgody rodziny [36].
Podejście to jest strategią zorientowaną na osobę, a nie na proces, i opiera się na umiejętnościach wyznaczonych wnioskodawców, aby wywołać altruizm wśród rodzin pogrążonych w żałobie. Na podstawie wyników autorzy zalecili, aby odpowiednie agencje rządowe skupiły się na szkoleniu pielęgniarek w celu omówienia dawstwa z rodzinami w żałobie i podniesienia świadomości społecznej [36].
Niemcy
Dawstwo narządów osiągnęło w Niemczech nowy poziom. Liczba dawców narządów spadła z 1296 w 2010 r. do zaledwie 797 dawców narządów w 2017 r. Oznacza to spadek o 916 przeszczepów nerek w ciągu ostatnich 6 lat (tab. III). Tym samym Niemcy zajmują przedostatnie miejsce w stowarzyszeniu Eurotransplant pod względem liczby dawców narządów na milion mieszkańców. Tylko Luksemburg ma mniej ze względu na odsetek obcokrajowców wynoszący 47,5%, a wielu z nich mieszka w sąsiednich krajach europejskich [37]. Jednak Niemcy są nie tylko daleko w tyle pod względem liczby dawców narządów w stowarzyszeniu Eurotransplant, lecz także na samym dole w porównaniu z innymi krajami europejskimi o porównywalnych strukturach politycznych, etycznych, religijnych i społecznych. Niemcy są krajem o jednym z najlepszych systemów opieki zdrowotnej na świecie, ale nie w dziedzinie dawstwa narządów. Nie ma jednego i ogólnego rozwiązania tego problemu. Istnieje wiele różnych punktów do rozważenia i rozwiązania. Obejmują one edukację populacji, wskazanie woli oddania narządów lub ich odrzucenia, szkolenie lekarzy w zakresie rozpoznawania potencjalnych dawców narządów, wsparcie dla urzędników transplantacyjnych i wiele innych. W szczególności jednak należy zastanowić się nad rozwiązaniem opt-out (domniemanej zgody). Minister Jens Spahn przyznał w rozmowie z gazetą „Bild”, że proponowane przez niego domniemanie zgody stanowi ingerencję państwa w wolność jednostki, ale wszystkie inne próby rozwiązania problemu spadającej liczby dawców nie przyniosły poprawy sytuacji. „Dlatego potrzebujemy szerokiej publicznej debaty o domniemaniu zgody” – powiedział Spahn [38].
Szybki rozwój bankowości tkanek i związanych z nią organizacji międzynarodowych nastąpił po upadku muru berlińskiego w 1991 r. Ten gwałtowny wzrost współpracy doprowadził do ogólnoświatowego konstruktywnego ruchu na rzecz wykorzystania i produkcji ludzkich tkanek. W miarę upływu lat industrializacja, prowadzona przez Stany Zjednoczone, poprawiła jakość aloprzeszczepów tkanek, ale doprowadziła do wyższych kosztów i konsolidacji w rozwijającym się przemyśle [7, 39, 40].
Prawo do wyrażenia zgody (opt-in) oraz prawo do rezygnacji (opt-out)
W niniejszym artykule stwierdzono, że istnieje niewielka różnica między systemami dawstwa narządów typu opt-in i opt-out w celu zwiększenia liczby dawców, gdy są one stosowane w izolacji. Niezależne przejście na system opt-out nie przynosi żadnych oczywistych korzyści i może zaszkodzić wysiłkom na rzecz zwiększenia darowizn. Konieczne jest raczej usunięcie barier dla dawstwa narządów na kilku poziomach wraz z przejściem do systemu. Ponadto dla wielu krajów korzystniejsze może być odpowiednie ubezwłasnowolnienie już istniejącego systemu dawstwa niż wprowadzanie znaczących zmian w związanym z nim zapotrzebowaniu na zasoby. Przez dziesięciolecia międzynarodowa społeczność transplantologiczna była zaangażowana w ożywioną debatę na temat zalet przejścia od domyślnych systemów opt-in do polityki opt-out w celu zwiększenia liczby dawców narządów i lepszego zaspokojenia stale rosnącego zapotrzebowania na przeszczepy ratujące życie. Opt-out jest z pewnością w modzie, ponieważ Walia, Anglia i Nowa Szkocja niedawno zdecydowały się na zmianę na opt-out, Szkocja ma zostać opt-out w marcu 2021 r., a Irlandia Północna i Kanada poważnie rozważają podobny ruch. Dzięki temu, że w ciągu ostatnich 20–30 lat kilka krajów przeszło z opt-in na opt-out, istnieją zestawy solidnych danych dotyczących zmian w czasie, które pomagają w analizie skuteczności systemów dawstwa. Jednak dane te są często sprzeczne i w dużej mierze niejednoznaczne, co sugeruje, że w grę mogą wchodzić inne czynniki. W niniejszym dokumencie dokonano przeglądu niektórych pojawiających się trendów w polityce dobrowolnego i opt-out w zakresie dawstwa narządów i rozważono najnowsze dane, które wyjaśniają niektóre z głównych sporów w każdym z nich. Szczegółowo omówiono ramy etyczne leżące u podstaw systemów dawstwa, takie jak świadoma zgoda, zaufanie i przejrzystość. Dużo czasu poświęca się również systemom opt-in vs opt-out w krajach rozwijających się, które są zwykle wyłączone z wielu analiz i w których napotykane wyzwania są potęgowane przez ograniczenia społeczno-gospodarcze. Stanowi to poważną lukę w niedawno opublikowanej literaturze, ponieważ kraje rozwijające się często pozostają daleko w tyle za swoimi rozwiniętymi odpowiednikami pod względem liczby dawców i przeszczepów [37, 38, 40].
Podsumowanie
Substytuty skóry mają na celu przyspieszenie gojenia się ran poprzez wymianę macierzy pozakomórkowej i mogą być stosowane do wspomagania gojenia zarówno ran ostrych, jak i przewlekłych [16, 41]. Alogeniczne biostatyczne przeszczepy skóry stanowią doskonały materiał tkankowy, stosowany w leczeniu pacjentów oparzonych i z ranami przewlekłymi. Podczas pobrania ze zwłok ludzkich uzyskuje się materiał tkankowy pozwalający na stworzenie znacznej rezerwy alogenicznych przeszczepów skóry, przygotowywanych i przechowywanych przez bank tkanek [10, 42].
Na podstawie danych rocznikowych opracowanych przez Krajowe Centrum Bankowania Tkanek i Komórek w Warszawie KCBTiK wykazano, że odsetek dawców skóry spoś́ród wszystkich dawców rzeczywistych wynosił 6,9% [43, 44]. Nie należy mieć żadnych wątpliwości, że taka ilość pobranej alogenicznej skóry ludzkiej nie jest w stanie zaspokoić rzeczywistego zapotrzebowania klinicznego na tego typu preparaty. Na stronie Poltransplantu oraz KCBTiK nie podano aktualnych danych dotyczących przeszczepiania skóry alogenicznej. Może to sugerować potrzebę uwzględniania danych dotyczących liczby pobrań oraz ilości pobranego materiału, jak również alokacji przygotowanych przeszczepów alogenicznej skóry.
Istnieje kilka procedur i ścieżek, które, jak wykazano, zapewniają praktyczne i skuteczne rozwiązania tego kryzysu. Można zaproponować kilka rozwiązań systemowych, m.in. wdrożenie odpowiednich programów edukacyjnych dla personelu publicznego i szpitalnego w zakresie potrzeby i korzyści płynących z dawstwa narządów ze szczególnym uwzględnieniem tkanek, propagowanie akceptacji koncepcji „domniemanej zgody”, wypracowanie altruistycznego systemu dawstwa od żywego dawcy na rzecz nieznanego biorcy [45]. Autorzy niniejszej pracy głęboko wierzą, że wdrożenie tych ścieżek pozyskiwania narządów od żywych i zmarłych dawców, przy odpowiednim uwzględnieniu kryteriów etycznych, religijnych i społecznych społeczeństwa, pozwoli wyeliminować kryzys niedoboru narządów oraz tkanek i wiele istnień ludzkich zostanie uratowanych dzięki procesowi dawstwa i przeszczepiania
narządów.
Wnioski
Przeszczepianie tkanek i narządów stanowi jedno z najważniejszych osiągnięć współczesnej medycyny. Niestety, problem deficytu dawców skóry alogenicznej jest rzadko poruszany w literaturze. Podczas gdy badacze poruszają temat potrzeby donacji narządów, niewiele źródeł literaturowych zwraca uwagę na to, że rezerwy ludzkich alogenicznych przeszczepów skóry nie są wystarczające dla zapewnienia potrzeb klinicznych. Dlatego też problemy transplantologii tkankowej ze szczególnym uwzględnieniem skóry stały się przewodnim tematem niniejszego artykułu ze względu na niski odsetek pobrań właśnie skóry.
Oświadczenie
Autorzy deklarują brak konfliktu interesów.
Piśmiennictwo
- Kamiński A. Przeszczepy tkankowe i komórkowe. W: Czerwiński J, Małkowski P (red.). Medycyna transplantacyjna dla pielęgniarek. PZWL, Warszawa 2017, str. 563–576.
- Corsi CAC, Shoji M, Scarpelini KCG i wsp. Implementation and certification of ISO 9001:2015 seal in human tissue bank HCFMRP-USP. Cell Tissue Bank 2020; 21: 563–571. DOI: 10.1007/s10561-020-09852-1.
- Khan AA, Khan IM, Nguyen PP i wsp. Skin Graft Techniques. Clin Podiatr Med Surg. 2020; 37: 821–835. DOI: 10.1016/j.cpm.2020.07.007.
- Phillips GO. The emergence and pitfalls of international tissue banking. Cell Tissue Bank 2018; 19: 167–173. DOI: 10.1007/s10561-018-9696-z.
- Dziedzic-Gocławska A, Kamiński A. Biostatyczne przeszczepy tkankowe. W: Rowiński W, Wałaszewski J, Pączek L (red.). Transplantologia kliniczna. PZWL, Warszawa 2004; 609–611 i 617–623.
- Łabuś W, Kawecki M, Nowak M. Rola inżynierii tkankowej w leczeniu ran oparzeniowych. Polski Przegląd Chirurgiczny 2012; 84: 284–291.
- Dörr B, Zeh RM, Rodriguez Torres LM, Stoyanov JV. Regulatory Challenges to Swiss Biobanks: A Qualitative Study. Praxis (Bern 1994) 2019; 108: 205. DOI: 10.1024/1661-8157/a003190.
- Uhrynowska-Tyszkiewicz I. Biostatyczne przeszczepy tkankowe. W: Rolka H, Kowalewska B, Jankowiak B, Krajewska-Kułak E (red.). Transplantologia i pielęgniarstwo transplantacyjne. PZWL, Warszawa 2017; 302–362.
- Blaise O, Duchesne C, Banzet S i wsp. A Murine Model of a Burn Wound Reconstructed with an Allogeneic Skin Graft. J Vis Exp 2020; (162): 10.3791/61339. DOI: 10.3791/61339.
- Klama-Baryła A, Łabuś W, Kraut M i wsp. Zastosowanie przygotowanych w banku tkanek przeszczepów tkankowych i komórkowych w leczeniu oparzeń oraz ran przewlekłych. Chir Pla Oparz 2019; 7: 9–16.
- Akbarzadeh S, McKenzie MB, Rahman MM, Cleland H. Allogeneic Platelet-Rich Plasma: Is It Safe and Effective for Wound Repair? Eur Surg Res 2021; 62: 1–9. DOI: 10.1159/000514223.
- Kaufhold-Wedel C, Hummel M, Brobeil A i wsp. Qualitätssicherung im Gewebebiobanking – Ein Überblick [Quality assurance in tissue biobanking-an overview]. Pathologie (Heidelb) 2022; 43: 365–371. DOI: 10.1007/s00292-022-01078-0.
- Dai C, Shih S, Khachemoune A. Skin substitutes for acute and chronic wound healing: an updated review. J Dermatolog Treat 2020; 31: 639–648. DOI: 10.1080/09546634.2018.1530443.
- Strong DM. Tissue banking, biovigilance and the notify library. Cell Tissue Bank 2018; 19: 187–195. DOI: 10.1007/s10561-017-9639-0.
- Klama-Baryła A, Kitala D, Łabuś W i wsp. Autologous and Allogeneic Skin Cell Grafts in the Treatment of Severely Burned Patients: Retrospective Clinical Study. Transplant Proc 2018; 50: 2179–2187. DOI: 10.1016/j.transproceed.2017.11.079.
- Przekora A. A Concise Review on Tissue Engineered Artificial Skin Grafts for Chronic Wound Treatment: Can We Reconstruct Functional Skin Tissue In Vitro? Cells 2020; 9: 1622. DOI: 10.3390/cells9071622.
- Baltazar T, Merola J, Catarino C i wsp. Three Dimensional Bioprinting of a Vascularized and Perfusable Skin Graft Using Human Keratinocytes, Fibroblasts, Pericytes, and Endothelial Cells. Tissue Eng Part A 2020; 26: 227–238. DOI: 10.1089/ten.TEA.2019.0201.
- Holl J, Kowalewski C, Zimek Z i wsp. Chronic Diabetic Wounds and Their Treatment with Skin Substitutes. Cells 2021; 10: 655. DOI: 10.3390/cells10030655.
- Werner M, Wróblewski P, Kawecki M. Oparzenia – postępowanie w pierwszych godzinach. W: Guła P, Machała W (red.). Postępowanie w obrażeniach ciała w praktyce SOR. PZWL, Warszawa 2017; 599–614.
- Snyder D, Sullivan N, Margolis D, Schoelles K. Skin Substitutes for Treating Chronic Wounds. Rockville (MD): Agency for Healthcare Research and Quality (US); February 2, 2020.
- Yusof N. Advances of radiation sterilisation in tissue banking. Cell Tissue Bank 2018; 19: 175–186. DOI: 10.1007/s10561-017-9651-4.
- Myint P. Radiation sterilisation and tissue banking. Cell Tissue Bank 2018; 19: 155–156. DOI: 10.1007/s10561-018-9705-2.
- Harrison DK, Waldrip ZJ, Burdine L, Shalin SC, Burdine MS. DNA-PKcs Inhibition Extends Allogeneic Skin Graft Survival. Transplantation 2021; 105: 540–549. DOI: 10.1097/TP.0000000000003442.
- Abouna GM. Organ shortage crisis: problems and possible solutions. Transplant Proc. 2008; 40: 34–38. DOI: 10.1016/
j.transproceed.2007.11.067. - Organ Donation and Transplantation Activity Report 2018-19. NHS Blood and Transplant.2019. Available at: https://nhsbtdbe.blob.core.windows.net/umbraco-assets-corp/16537/organ-d… [dostęp: 9.06.2023].
- Manara AR, Thomas I. Current status of organ donation after brain death in the UK. Anaesthesia 2020; 75: 1205–1214. DOI: 10.1111/anae.15038.
- Nather A, Mandy FSY, Ning T, Kaiying W. Tissue banking in Asia Pacific region: past, present and future. Cell Tissue Bank 2018; 19: 229–240. DOI: 10.1007/s10561-018-9697-y.
- Li AH, McArthur E, Maclean J i wsp. Deceased Organ Donation Registration and Familial Consent among Chinese and South Asians in Ontario, Canada. PLoS One 2015; 10: e0124321. DOI: 10.1371/
journal.pone.0124321. - Lobo Gajiwala A. Regulatory aspects of tissue donation, banking and transplantation in India. Cell Tissue Bank 2018; 19: 241–248. DOI: 10.1007/s10561-018-9689-y.
- Rhee J, Kern B, Cooper J, Freeman RB. Organ donation. Semin Liver Dis 2009; 29: 19–39. DOI: 10.1055/s-0029-1192053.
- Etheredge HR. Assessing Global Organ Donation Policies: Opt-In vs Opt-Out. Risk Manag Healthc Policy 2021; 14: 1985–1998. DOI: 10.2147/RMHP.S270234.
- Fabian J, Crymble K. End-of-life care and organ donation in South Africa – it’s time for national policy to lead the way. S Afr Med J 2017; 107: 11947. DOI: 10.7196/SAMJ.2017.v107i7.12486.
- Pullen LC. Transplantation in Africa. Am J Transplant 2017; 17: 1431–1432. DOI: 10.1111/ajt.14331.
- Thomson D. Getting better – health profession knowledge is key to improving deceased donation practices in South Africa. South Afr J Crit Care 2019; 35: 10.7196/SAJCC.2019.v35i2.414. DOI: 10.7196/SAJCC.2019.v35i2.414.
- Bookholane H, Michaelides A, Prins L i wsp. Factors influencing consent rates of deceased organ donation in Western Cape Province, South Africa. S Afr Med J 2020; 110: 204–209. DOI: 10.7196/SAMJ.2020.v110i3.14227.
- Naghavi N, Mubarik MS, Rasiah R, Sharif Nia H. Prioritizing Factors Affecting Deceased Organ Donation in Malaysia: Is a New Organ Donation System Required? Int J Gen Med 2020; 13: 641–651. DOI: 10.2147/IJGM.S253372
- Weigand K. Organspende in Deutschland: Wollen wir nicht? Können wir nicht? Oder dürfen wir nicht? [Organ donation in Germany: Don’t we want to? Can’t we? Or are we not allowed?]. Urologe A 2018; 57: 1091–1099. DOI: 10.1007/s00120-018-0734-z.
- Domniemana zgoda na pobranie organów w Niemczech. Menedżer Zdrowia [dostęp: 9.06.2023].
- Phillips GO. The emergence and pitfalls of international tissue banking. Cell Tissue Bank 2018; 19: 167–173. DOI: 10.1007/s10561-018-9696-z.
- Biblioteka raportów statystycznych Eurostransplant: www.Eurotransplant – Statistics.org [dostęp: 9.06.2023].
- Jayarajan S, Meissler JJ, Adler MW, Eisenstein TK. A Cannabinoid 2-Selective Agonist Inhibits Allogeneic Skin Graft Rejection In Vivo. Front Pharmacol 2022; 12: 804950. DOI: 10.3389/fphar.2021.804950.
- Mandujano-Tinoco EA, González-García F, Salgado RM i wsp. miR-31, miR-155, and miR-221 Expression Profiles and Their Association With Graft Skin Tolerance in a Syngeneic vs Allogeneic Murine Skin Transplantation Model. J Burn Care Res 2022; 43: 1160–1169. DOI: 10.1093/jbcr/irac003.
- Zestawienie zbiorcze aktywności ośrodków zajmujących się bankowaniem tkanek i komórek w zakresie donacji za rok 2016 http://www.kcbtik.pl/zestawienia/bt2016.pdf [dostęp: 9.06.2023].
- Łabuś W, Kitala D, Navarro A i wsp. The urgent need to achieve an optimal strategic stock of human allogeneic skin graft materials in case of a mass disaster in Poland. Cell Tissue Bank 2022; 23: 863–885. DOI: 10.1007/s10561-022-10001-z.
- de Almeida GP, Lichtner P, Eckstein G i wsp. Human skin-resident host T cells can persist long term after allogeneic stem cell transplantation and maintain recirculation potential. Sci Immunol 2022; 7: eabe2634. DOI: 10.1126/sciimmunol.abe2634.

