Wytyczne | Guidelines
Stanowisko Polskiego Towarzystwa Leczenia Ran – postępowanie przeciwdrobnoustrojowe w ranie skolonizowanej, z cechami infekcji i zagrożonej infekcją w erze antybiotykooporności
Statement of the Polish Wound Management Association – antimicrobial management in colonized wounds, with signs of infection and at risk of infection in the era of antibiotic resistance
Maciej Sopata1, Beata Mrozikiewicz-Rakowska![]() 2, Arkadiusz Jawień
2, Arkadiusz Jawień![]() 3, 4, Jarosław Woroń
3, 4, Jarosław Woroń![]() 5, Marcin Malka
5, Marcin Malka![]() 6, Tomasz M. Karpiński
6, Tomasz M. Karpiński![]() 7, Anna Sobieszek-Kundro
7, Anna Sobieszek-Kundro![]() 8, Marcin Gabriel9, Przemysław Mańkowski
8, Marcin Gabriel9, Przemysław Mańkowski![]() 10, Maria T. Szewczyk
10, Maria T. Szewczyk![]() 11, Helena Jastrzębska2, Monika Aleksy-Polipowska12, Paulina Mościcka
11, Helena Jastrzębska2, Monika Aleksy-Polipowska12, Paulina Mościcka![]() 11
11
1 Pracownia Leczenia Ran Przewlekłych, Katedra
i Klinika Medycyny Paliatywnej, Hospicjum Palium, Uniwersytet Medyczny im.
Karola Marcinkowskiego w Poznaniu, Polska
2 Klinika Endokrynologii, Centrum Medyczne Kształcenia
Podyplomowego w Warszawie, Polska
3 Katedra i Klinika Chirurgii Naczyniowej
i Angiologii, Collegium Medicum im. Ludwika Rydygiera
w Bydgoszczy, Uniwersytet Mikołaja Kopernika w Toruniu, Polska
4 Szpital Uniwersytecki nr 1 im. dr. A. Jurasza
w Bydgoszczy, Polska
5 Zakład Farmakologii Klinicznej, Katedra Farmakologii,
Wydział Lekarski, Uniwersytet Jagielloński Collegium Medicum w Krakowie,
Polska
6 Klinika Leczenia Ran PODOS w Warszawie, Polska
7 Katedra i Zakład Mikrobiologii Lekarskiej,
Uniwersytet Medyczny im. Karola Marcinkowskiego w Poznaniu, Polska
8 Oddział Dermatologiczny, Wojewódzki Szpital Zespolony
w Elblągu, Polska
9 Klinika Chirurgii Naczyniowej, Wewnątrznaczyniowej,
Angiologii i Flebologii, Uniwersytet Medyczny im. Karola Marcinkowskiego
w Poznaniu, Polska
10 Katedra i Klinika Chirurgii, Traumatologii
i Urologii Dziecięcej, Uniwersytet Medyczny w Poznaniu, Polska
11 Zakład Pielęgniarstwa Chirurgicznego i Leczenia Ran
Przewlekłych, Katedra Pielęgniarstwa Zabiegowego, Collegium Medicum
im. Ludwika Rydygiera w Bydgoszczy, Uniwersytet Mikołaja Kopernika
w Toruniu, Polska
12 Kamiliańskie Centrum Opieki Paliatywnej
w Tarnowskich Górach
Adres do korespondencji
dr hab. n. med. Maciej Sopata, Pracownia Leczenia Ran Przewlekłych, Katedra i Klinika Medycyny Paliatywnej, Hospicjum Palium, Uniwersytet Medyczny w Poznaniu, os. Rusa 55, 61-245 Poznań, e-mail: maciej.sopata@skpp.edu.pl
Nadesłano: 10.12.2023
Zaakceptowano: 14.12.2023
Opublikowano: 30.12.2023
LECZENIE RAN 2023; 20 (4): 125–141
DOI: 10.60075/lr.v20i4.59
Spis treści:
Wprowadzenie
Leczenie ran trudno gojących w czasie postpandemicznym wydaje się jeszcze większym globalnym wyzwaniem niż dotychczas. Utrudniony podczas pandemii kontakt z personelem medycznym, w tym ograniczenie wizyt w gabinetach zabiegowych czy w domu pacjenta, oraz odraczanie terminów zaplanowanych zabiegów chirurgicznych przyczyniły się do pogorszenia stanu zdrowia pacjentów, w tym stanu ran trudno się gojących. Brakuje obecnie statystyk dotyczących amputacji kończyn dolnych oraz danych dotyczących zgonów pośrednio związanych z pogorszeniem stanu pacjenta, np. wskutek infekcji wstępującej i sepsy.
Głównymi przyczynami utrudniającymi proces gojenia się ran trudno gojących się są biofilm bakteryjny i infekcja rany [1–4]. Z opublikowanego przez Światową Organizację Zdrowia (World Health Organization – WHO) i Europejskie Centrum ds. Zapobiegania i Kontroli Chorób (European Centre for Disease Prevention and Control – ECDC) raportu dotyczącego antybiotykooporności drobnoustrojów wynika, że obserwujemy wzrost liczebności szczepów opornych na antybiotyki, w tym na antybiotyki ostatniej linii, np. karbapenemy [5]. Dane te dotyczą również Europy Środkowej oraz Polski [5]. Stosowanie nieracjonalnej antybiotykoterapii empirycznej nie tylko w przypadku infekcji owrzodzeń, lecz także w przypadku infekcji np. górnych dróg oddechowych czy zakażeń układu moczowego przyczynia się do obecnego stanu rzeczy. Niepokojąca jest ilość szczepów wielolekoopornych (multidrug-resistant organisms – MDRO) izolowanych obecnie z ran trudno gojących się, np. odleżyn, owrzodzeń w zespole stopy cukrzycowej, owrzodzeń goleni, oparzeń czy ran nowotworowych. Zjawisko to dotyczy również powikłań rany pooperacyjnej i zakażenia miejsca operowanego, które wpisuje się w definicję zakażeń związanych z opieką zdrowotną (hospital aquired infections – HAI). Zakażenia związane z opieką zdrowotną mogą dotyczyć nawet 38% pacjentów hospitalizowanych na oddziałach intensywnej opieki medycznej, z czego ok. 18% może dotyczyć zakażenia miejsca operowanego lub zakażenia płuc i w obu przypadkach jest związane z występowaniem drobnoustrojów wielolekoopornych [6].
System ochrony zdrowia wymaga wsparcia w tym zakresie i zwrócenia uwagi na zwiększające się ryzyko braku skutecznej antybiotykoterapii. Międzynarodowe organizacje, takie jak Europejskie Towarzystwo Leczenia Ran (European Wound Management Association – EWMA) czy Międzynarodowy Instytut ds. Zakażeń w Ranach (International Wound Infection Institute – IWII), zajmujące się leczeniem ran, opublikowały ostatnio zalecenia uzupełniające wytyczne postępowania z ranami w świetle rosnącej antybiotykoodporności [1, 4]. Dodatkowo w odpowiedzi na nadal pogarszającą się sytuację powołano Grupę Ekspertów, która opublikowała w 2023 r. konsensus antyseptyki, w ramach którego przedstawiła obecny stan, obawy i propozycje rozwiązań dotyczące stosowania środków antyseptycznych w praktyce w celu zapobiegania i leczenia infekcji ran w erze antybiotykoodporności [7].
Celem niniejszego dokumentu jest aktualizacja wytycznych Polskiego Towarzystwa Leczenia Ran (PTLR) z 2020 r. o stanowiska międzynarodowe dotyczące stosowania substancji o działaniu bójczym w leczeniu ran trudno gojących się, tj. konsensus dotyczący użycia antyseptyków w praktyce autorstwa Harikrishny K.R. Naira i wsp. z 2023 r. [7], zalecenia stosowania środków przeciwdrobnoustrojowych w leczeniu ran trudno gojących się – EWMA 2022 [4], najlepsze praktyki terapii ran z cechami infekcji opublikowane przez IWII w 2022 r. (IWII Wound Infection Continuum) [1].
Polskie Towarzystwo Leczenia Ran, mając na uwadze globalny program ochrony antybiotyków oraz prognozy WHO, NICE oraz ECDC [8–10] co do dostępności i skuteczności antybiotykoterapii w przyszłości, składa w Państwa ręce poniższą aktualizację wytycznych PTLR opublikowanych w 2020 r. Dokument ten zwraca szczególną uwagę na zasadne stosowanie produktów z substancją przeciwdrobnoustrojową, tj. antyseptyków, produktów do płukania ran (lawaseptyków), opatrunków specjalistycznych z substancją bójczą z uwzględnieniem zasad aseptycznej pracy, w tym racjonalnej dezynfekcji powierzchni oraz higieny rąk. Zgodnie z zasadą „lepiej zapobiegać niż leczyć” zwracamy uwagę na konieczność walki z antybiotykoopornością poprzez standaryzowane i racjonalne stosowanie środków przeciwdrobnoustrojowych (antimicrobial stewardship – AMS), w tym antybiotyków.
Rana trudno gojąca się – wyzwania w erze antybiotykoodporności
Pomimo rozwoju nauk biomedycznych, dostępu do innowacyjnej diagnostyki i terapii ran oraz intensyfikacji edukacji personelu medycznego oraz pacjentów i ich opiekunów problem ran trudno gojących jest nadal wyzwaniem, szczególnie po okresie pandemii COVID-19. Rany trudno gojące się, do których należą odleżyny, owrzodzenia w zespole stopy cukrzycowej, owrzodzenia żylne goleni, powikłane oparzenia i rany pooperacyjne oraz rany nowotworowe, cechuje przewlekły stan zapalny, kolonizacja drobnoustrojami, a dokładniej biofilmem (60–100%) oraz brak tendencji do samoistnego gojenia ze względu na etiopatogenezę i chorobę podstawową. Definicja wg Murphy wskazuje również, że rany te nie reagują na leczenie zgodne ze standardami i momentem kluczowym w zakwalifikowaniu ich jako trudno gojących się jest 3. dzień, w którym rana wykazuje zwiększony wysięk, włóknik w dnie rany i zwiększenie jej rozmiaru [2, 3]. Częstość występowania na świecie ran trudno gojących się o mieszanej etiologii wynosi 2,21 na 1000 mieszkańców [4]. Liczba chorych ciągle wzrasta, do czego przyczyniają się m.in. starzejące się społeczeństwo, zmieniający się tryb życia oraz coraz częstsze występowanie chorób cywilizacyjnych, takich jak cukrzyca, otyłość, zespół metaboliczny, niewydolność żylna, miażdżyca, choroby nowotworowe. Szacuje się, że w Polsce może być nawet ok. 500 tys. pacjentów z ranami przewlekłymi. Stanowią oni poważne obciążenie społeczne i finansowe nie tylko dla osób dotkniętych chorobą, lecz także dla ich rodzin i otoczenia oraz systemów opieki zdrowotnej [11].
Lepiej zapobiegać niż leczyć – strategia zarządzania środkami przeciwdrobnoustrojowymi jako element ochrony antybiotyków i antyseptyków
Czynnikiem zakłócającym i wydłużającym czas leczenia oraz prowadzącym do wielu powikłań jest infekcja rany, której w większości przypadków można zapobiec poprzez prawidłową, powtarzalną strategię AMS. Celem strategii AMS, która została szczegółowo przedstawiona w konsensusie antyseptyki opublikowanym przez Naira i wsp. w 2023 r., uzasadnione i racjonalne jest stosowanie substancji bójczych nie tylko w ramach walki z infekcją, ale przede wszystkim w ramach profilaktyki oraz ochrony antybiotyków. W tabeli I przedstawiono główne zagadnienia niezbędne do wdrożenia i realizacji strategii AMS w walce z rosnącą opornością na substancje przeciwdrobnoustrojowe, w tym antybiotyki i antyseptyki [7].

Obciążenie mikrobiologiczne w ranie – definicje
Mając na uwadze rosnącą oporność drobnoustrojów na środki przeciwdrobnoustrojowe (antimicrobial resistance – AMR), w tym antybiotyki, oraz zalecenia międzynarodowych grup eksperckich, takich jak EWMA, IWII i WHO, w terapii ran trudno gojących się należy szczególną uwagę zwrócić na równowagę mikrobiologiczną w ranie, czyli na ilość występujących drobnoustrojów (miano), ich zjadliwość oraz stan pacjenta, w tym stan jego układu immunologicznego [1, 4, 7, 11]. Poziom obciążenia mikrobiologicznego oraz stan równowagi w ranie determinuje podjętą terapię. Konsensus antyseptyki Naira i wsp., stanowisko IWII z 2022 r. oraz obserwacje własne wskazują na pilną potrzebę doprecyzowania terminów stosowanych przy ocenie stanu równowagi mikrobiologicznej rany.
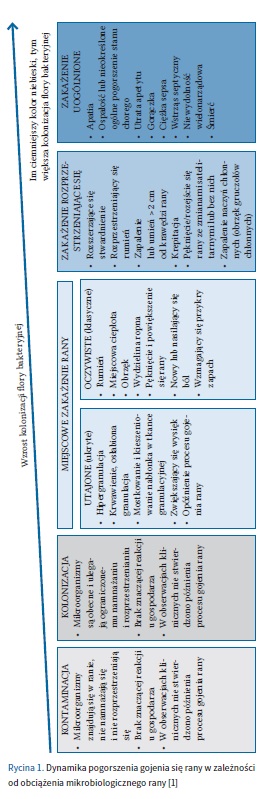
W 2022 r. termin „krytyczna kolonizacja” został wycofany i zastapiony terminem „infekcja miejscowa” [1]. Infekcja miejscowa umożliwia rozróżnienie jej na utajoną i pełnoobjawową. Wstępna faza zakażenia, często nazywanego zakażeniem utajonym, charakteryzuje się np. tworzeniem kieszeni, mostkowaniem, stwardnieniem tkanki i hipergranulacją. Te cechy kliniczne często nie są odnotowywane, a ich rozwój prowadzi do cech jawnej infekcji, którą charakteryzuje zaczerwienienie lub rumień, wzrost ocieplenia, obrzęk, wydzielina ropna, zastój gojenia, zwiększenie odczuć bólowych i nasilający się nieprzyjemny zapach. Termin „miejscowe zakażenie rany” jest obecnie powszechnie akceptowany. Trudno jest precyzyjnie zdefiniować termin „zakażenie rany” i odróżnić je od masywnej kolonizacji. Potrzeba doprecyzowania dotyczy również terminów: „kontaminacja”, „kolonizacja”, „rana z biofilmem” i „rana objęta zakażeniem miejscowym” czy „ rozprzestrzeniającym się” (ryc. 1). Zgodnie z dokumentem IWII każda rana jest skolonizowana [1]. Kolonizacja nie musi być równoznaczna z infekcją, aczkolwiek może do niej prowadzić. Według IWII zakażenie w ranie to „zasiedlenie rany przez namnażające się mikroorganizmy, co w efekcie wywołuje miejscową i/lub uogólnioną odpowiedź gospodarza” [1]. Rana skolonizowana może być przez formy planktoniczne drobnoustrojów lub poprzez wysoko wyspecjalizowany ekosystem obecny w 60–100% owrzodzeń, czyli biofilm [1, 2, 4, 7].
Biofilm to złożony wielogatunkowy ekosystem drobnoustrojów zamkniętych w zewnątrzkomórkowej substancji polimerowej – matrix. Struktura ta wykazuje zdolność przyczepiania się do powierzchni żywych, np. ziarniny, naskórka czy błon śluzowych, lub martwych, np. nici chirurgicznej, implantów, zwiększając prawdopodobieństwo zakażenia i uniemożliwiając proces gojenia [12, 13]. Gdy liczebność drobnoustrojów w biofilmie osiąga poziom krytyczny mierzony poprzez system kontroli liczebności, tzw. quorum sensing (QS), drobnoustroje zmieniają swoje cechy, np. uruchamiając nowe szlaki metaboliczne, specjalizując się, zmieniając swoje właściwości np. w oporności czy wydzielaniu toksyn [14]. Niektóre bakterie zwalniają procesy życiowe, przechodząc w formy wegetatywne, niewrażliwe na substancje bójcze. Kluczową cechą biofilmu jest jego niewrażliwość na działanie układu immunologicznego, odporność na działanie silnych substancji o działaniu bójczym, w tym produktów do dezynfekcji. Zawieszone w ochronnej warstwie matrix drobnoustroje, wyeksponowane na pojedyncze cząsteczki, np. antybiotyków, działają jak złożona maszyneria produkująca geny oporności. Działania przeciwbiofilmowe bazują głównie na mechanicznym usunięciu struktury matrix oraz niedopuszczaniu do odbudowy postaci dojrzałej [1, 2]. Należy mieć na uwadze, że biofilm ma zdolność odbudowania swojej struktury w kilkanaście godzin, a po 3 dobach może mieć już postać dojrzałą [2, 14]. Znajomość wyżej opisanych terminów jest niezbędna do komunikacji między personelem oraz między personelem a pacjentem i gwarantuje obranie właściwej strategii terapeutycznej.
Diagnostyka mikrobiologiczna rany
Postawienie diagnozy zakażenia w ranie jest często możliwe dzięki połączeniu oceny klinicznej i badań mikrobiologicznych [15, 16]. Głównym wyzwaniem w ocenie klinicznych objawów zakażenia w ranie pozostaje subiektywność, ponieważ objawy te manifestują się w różny sposób – w zależności od rodzaju rany i chorób współistniejących, a czasem również od kondycji psychicznej pacjenta. Opisana szczegółowo w wytycznych PTLR diagnostyka mikrobiologiczna jest nadal aktualna i obowiązująca. Należy jednak zwrócić uwagę na sposób pobierania materiału mikrobiologicznego z rany. To, co jest bezdyskusyjne, to wstępne przygotowanie łożyska rany (wound bed preparation – WBP), które obowiązuje przy każdej zmianie opatrunku. Celem WBP, łączącego elementy strategii TIME, TIMERS i higieny rany, jest stworzenie wilgotnego środowiska, które optymalizuje warunki oczyszczania i gojenia rany poprzez tworzenie dobrze unaczynionego, stabilnego łożyska rany, zmniejszenia obciążenia bakteryjnego, ograniczenia produkcji wysięku i przyśpieszenia tworzenia ziarniny [1, 2, 4, 7, 11] (ryc. 2).

Zgodnie z powyższym przed pobraniem materiału łożysko rany należy dokładnie oczyścić. Dobre praktyki sugerują, aby po zdjęciu opatrunku oczyścić również skórę wokół rany w celu zmniejszenia ryzyka kontaminacji ze skóry otaczającej. Można do tego celu stosować produkty do pielęgnacji i dekontaminacji skóry, np. w postaci rękawic czy chusteczek, zawierające oktenidynę (OCT), poliheksanidynę (PHMB), chlorheksydynę (CHX) bądź zwykłe rękawice lub pianki pielęgnująco-myjące do skóry nieuszkodzonej. Planując pobranie materiału do analizy mikrobiologicznej, należy pamiętać o odpowiednich produktach do oczyszczania łożyska rany. Decydując się na pobranie materiału do analizy mikrobiologicznej, nie można stosować produktów z substancją bójczą, gdyż zakłóci to wynik. Łożysko rany powinno zostać oczyszczone z tkanki martwiczej, martwicy rozpływnej, włóknika, strupów [17, 18].
Należy zadbać również o usunięcie niewidocznego gołym okiem biofilmu, który w fazie dojrzałej może manifestować się połyskującą warstwą śluzu. W tym celu należy oczyścić mechanicznie łożysko rany (nawet ziarninę) z wykorzystaniem soli fizjologicznej, płynu Ringera lub wody do wstrzykiwań oraz sterylnych czyścików, które usuną dokładnie biofilm i zanieczyszczenia.
Technika pobierania materiału do analizy mikrobiologicznej i antybiogramu zależy od rodzaju rany, choroby podstawowej i kwalifikacji personelu.Zgodnie z stanowiskiem IWII z 2022 r. i EWMA z 2022 r. zaleca się pobieranie materiału w postaci bioptatów tkankowych. Należy zaznaczyć, że w konsensusie antyseptyki z 2023 r. zwrócono uwagę, że z powodu kosztów, umiejętności, uprawnień i ograniczeń czasowych i transportowych zamiast biopsji tkanek nadal częściej pobierane są wymazy z ran. Ich wartość diagnostyczna ma miejsce pod warunkiem prawidłowo przeprowadzonej procedury [17–19]. Szczególnie w przypadku podejrzenia izolatów wielolekoopornych oraz zakażenia uogólnionego i dynamicznie postępujących zmian, jak np. w zespole stopy cukrzycowej, zaleca się pobranie bioptatu. Standardową techniką stosowaną do pobrania posiewu, szczególnie w zespole stopy cukrzycowej, powinna być biopsja tkankowa (deep-tissue biopsy), rekomendowana przez autorów IWGDF jako najlepsza procedura diagnostyczna [17]. Stosując tę metodę, posiew można pobierać przy użyciu igły do biopsji gruboigłowej, łyżki typu Volkmanna lub odgryzacza kostnego typu Luer. W przypadku posiewów uzyskiwanych z kości, tkankę kostną zaleca się pobierać przy użyciu odgryzacza kostnego typu Luer. Pobrany materiał należy przenieść z narzędzia na podłoże transportowe przy użyciu aplikatora z wacikiem wiskozowym będącym elementem składowym podłoża transportowego. W literaturze często jako argument przeciwko biopsji gruboigłowej podawany jest zwiększony koszt procedury lub ból związany z samą procedurą. Ciężko uznać ten argument za trafny, biorąc pod uwagę, że narzędzia stosowane do wykonania biopsji tkankowej są tymi samymi, które stosujemy do oczyszczenia czy diagnostyki histopatologicznej rany. Podobnie potencjalny ból związany z pobraniem materiału do badania mikrobiologicznego powinien już wcześniej być opanowany w celu odpowiedniego oczyszczenia łożyska rany. Biorąc pod uwagę, jak istotne jest uzyskanie wiarygodnej wiedzy na temat patogenów odpowiadających za zakażenia rany trudno gojącej się, autorzy mają na celu promocję ww. techniki. W wybranych przypadkach, np. w ranach, w przypadku których zastosowanie metody biopsji tkankowej nie było możliwe z powodu małej wielkości rany lub braku odpowiednich warunków (opieka środowiskowa, ograniczone możliwości narzędziowe), dopuszczalne jest zastosowanie techniki Levina, polegającej na wymazie z powierzchni rany przez obracanie lub rolowanie wymazówki na obszarze 1–2 cm2 przez kilka sekund, naciskając przy tym na powierzchnię rany, tak aby uzyskać płyn tkankowy.
Istotnym czynnikiem decydującym o jakości wyniku badania mikrobiologicznego jest rodzaj użytego podłoża uwzględniający charakterystykę i rodzaj rany oraz miejsce pobrania materiału. Izolatów beztlenowych będziemy oczekiwać z zakażonych ran głębokich, z kieszeni, z przetok oraz z ran z martwicą. W przypadku podłoży typu Amies warto wziąć pod uwagę podłoża z węglem (czarny korek), w których materiał tlenowy jest stabilny aż do 96 godzin, a beztlenowy do 48 godzin. W przypadku podłoża bez węgla (niebieski korek) stabilność patogenów beztlenowych to jedynie 2 godziny. Może być to główny powód fałszywie ujemnych wyników badań w kierunku beztlenowców. W tabeli II przedstawiono materiał, jakiego nie powinno się pobierać do analizy mikrobiologicznej.

Celem analizy mikrobiologicznej nie jest ocena ilościowa i jakościowa drobnoustrojów, ale przede wszystkim wykonanie antybiogramu. Jeśli przed procedurą zastosowano antybiotykoterapię empiryczną, terapia powinna być zmieniona, zgodnie z wynikami antybiogramu (jeżeli nie ma postępu gojenia rany). Należy bezwzględnie pamiętać o niestosowaniu antybiotyków miejscowo w postaci np. maści oraz o holistycznym podejściu do pacjenta w aspekcie dobrania dawki antybiotyku. Holistyczne podejście uwzględnia współpracę zespołu składającego się z chirurga, mikrobiologa, farmaceuty oraz osoby oceniającej np. farmakokinetykę w aspekcie choroby podstawowej pacjenta, działań niepożądanych czy przeciwwskazań. Niezwykle ważne w powodzeniu terapii jest uwzględnienie zmniejszenie perfuzji naczyń tętniczych i ryzyko niedostarczenia odpowiedniej dawki celowej do ogniska infekcji [1, 4, 7, 11].
Oceny zaawansowania infekcji dokonujemy również z wykorzystaniem wyników badania krwi i biomarkerów infekcji. Do analizowanych parametrów należą morfologia z pełnym rozmazem, leukocytoza, odczyn Biernackiego (OB), białko C-reaktywne (CRP) i prokalcytonina (PCT). Trwają prace naukowców nad nowymi biomarkerami, w tym pobieranymi bezpośrednio z łożyska rany. Wskaźnikiem wskazującym na przekroczenie równowagi mikrobiologicznej i infekcję miejscową jest również podwyższona temperatura ciała wokół rany. Należy pamiętać, że wykorzystanie temperatury jako wskaźnika zakażenia może być trudne w przypadku niektórych chorób, takich jak miażdżyca tętnic obwodowych (chłodne dystalne fragmenty kończyn) . Potencjalnym wczesnym wskazaniem zakażenia może być również pH rany, dlatego jego monitorowanie może również być przydatnym narzędziem do określania obecności zakażenia [7]. W ranach niereagujących na terapię prowadzoną zgodnie z standardami należy uwzględnić diagnostykę procesu nowotworowego, który często jest rezultatem przewlekłego stanu zapalnego i objawia się najczęściej w postaci raka kolczystokomórkowego skóry. W przypadku niegojących się owrzodzeń żylnych goleni diagnostykę należy rozpocząć po 4–6 tygodniach terapii standardowej. Kluczowe jest w takiej sytuacji pobranie materiału na diagnostykę histopatologiczną z dokładnym jego opisaniem [11].
Postępowanie przeciwdrobnoustrojowe AMS
W 2022 r. EWMA oraz IWII wydały aktualizację zaleceń dotyczących postępowania z raną z infekcją [1, 4]. Głównym celem aktualizacji jest zwrócenie uwagi na prawidłowo dobraną terapię przeciw drobnoustrojom, okres jej trwania z szczególnym uwzględnieniem rozpoznania stanu równowagi mikrobiologicznej w ranie. Z uwagi na krytycznie rosnącą AMR w 2023 r. został opublikowany międzynarodowy konsensus antyseptyki skupiający się głównie na zasadach stosowania substancji przeciwdrobnoustrojowych [7]. Uważa się, że chronić należy nie tylko antybiotyki, ale również produkty o działaniu bójczym stosowane w terapiach miejscowych. Rosnąca oporność, w tym krzyżowa, np. na chlorheksydynę, skłania do rozważnego i racjonalnego stosowania substancji o działaniu przeciwdrobnoustrojowym.
Statystyki wskazują, że nadal istnieje tendencja do przepisywania nadmiernej ilości antybiotyków – szczególnie pacjentom z przewlekłymi ranami. Aż 16,4% recept na antybiotyki jest związanych z leczeniem ran [2]. Coraz więcej izolatów z owrzodzeń charakteryzuje się opornością na więcej niż jeden antybiotyk. Prawidłowa i racjonalna strategia AMS, prowadzona szczególnie u pacjentów wielokrotnie hospitalizowanych, powinna uwzględniać ewentualne ryzyko wystąpienia oporności nie tylko na antybiotyki, ale na inne substancje. Aktualnie coraz częściej pojawia się w piśmiennictwie termin „tolerancja drobnoustrojów na substancje bójcze”. Nie jest to cecha dziedziczna determinowana mechanizmem precyzyjnego ominięcia działania antybiotyku, np. poprzez zmianę budowy receptora dla antybiotyku lub wykorzystanie pompy wyrzucającej cząsteczkę czy obecność enzymów ją rozkładających, ale cecha fizycznego zaadaptowania nabytego podczas inkubacji w roztworach wielokrotnie rozcieńczonych. Kluczowe jest niemieszanie produktów zawierających substancje bójcze ani rozcieńczanie ich niezgodnie z instrukcją.
Nie stwierdzono genów oporności na jodopowidon (PVP-I) oraz cząsteczkę oktenidyny [20–22].
Status rejestracyjny produktów stosowanych w postępowaniu przeciwdrobnoustrojowym AMS
Każdy praktyk oraz pacjent powinien być zaznajomiony ze statusem rejestracyjnym produktów stosowanych w terapii. Wyróżnia się trzy statusy rejestracyjne produktów stosowanych u ludzi – leki, wyroby medyczne i produkty biobójcze. Rejestracja oraz status „produkt leczniczy” wiążą się z dokładnie sprecyzowanym profilem bezpieczeństwa wynikającym z przeprowadzonych wcześniej obligatoryjnie badań klinicznych, często w różnych grupach wiekowych, z precyzyjnie sformułowanymi wskazaniami terapeutycznymi i przeciwwskazaniami, sposobem i częstotliwością dawkowania. W charakterystyce produktu leczniczego (ChPL) są zawarte również „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania” oraz „Interakcje z innymi produktami leczniczymi” [23]. Leki mogą również być przebadane pod względem wpływu na płodność oraz stosowania w trakcie ciąży, wpływu na płód, laktację. W ChPL danego leku opisany jest też wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn, działania niepożądane oraz aspekty związane z przedawkowaniem. Szczegółowa charakterystyka produktów leczniczych ma wpływ na prawidłowe ich stosowanie z uwzględnieniem farmakokinetyki, farmakodynamiki, składu oraz „Przedklinicznych danych o bezpieczeństwie” [23]. Tak dokładne i precyzyjne dane przedstawione podczas procesu rejestracji wiążą się z specyficznym działaniem leków. Produkty lecznicze stosowane do odkażania ran działają w sposób farmakologiczny, metaboliczny i/lub immunologiczny, natomiast wyroby medyczne służące do przemywania ran działają jedynie w sposób fizyczny. Stosując lek – antyseptyk – zgodnie z lokalnym protokołem i ChPL, mamy wiedzę na temat potwierdzonej skuteczności przeciwdrobnoustrojowej w określonym czasie, wymaganym czasie kontaktu, sposobie aplikacji miejscowej i dawce. Dlatego przy wyborze produktu należy zwrócić uwagę na kategorie rejestracyjne produktu.
Wśród produktów do wspomagania leczenia ran, w tym zmniejszających obciążenie mikrobiologiczne w ranie, wyróżnia się również te o statusie wyrobów medycznych (medical devices – MD). Różnią się one głównie mechanizmem działania, a ich głównym zadaniem jest płukanie i nawilżanie łożyska ran [24]. Nazywane są lawaseptykami, czyli produktami do oczyszczania mechanicznego oraz przemywania (cleansing). Do klasycznych lawaseptyków zalicza się sól fizjologiczną oraz roztwór Ringera. Warto wspomnieć tu o produktach z surfaktantem, np. etyloheksylogliceryną lub betainą, które lepiej radzą sobie przy mechanicznym myciu ran z użyciem czyścików oraz o produktach nieuszkadzających chrząstki i bezpiecznych do podawania do kieszeni i jam ciała (podchloryny o niskim stężeniu).
Oczyszczanie (debridement) rany warunkiem skutecznego postępowania AMS
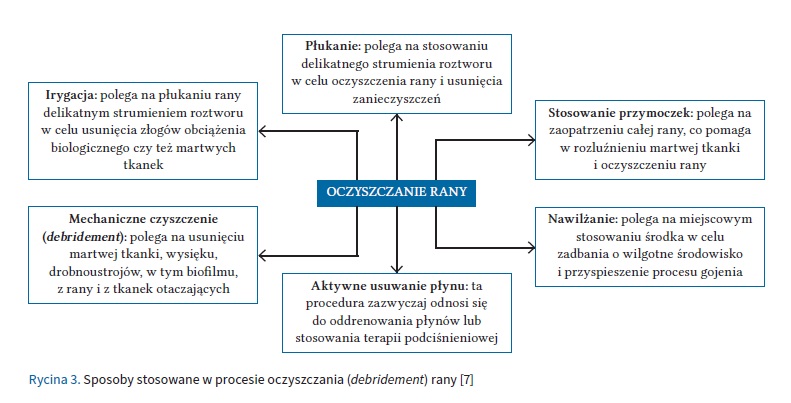
Stosowanie lawaseptyków odgrywa główną rolę w tzw. szeroko pojętym oczyszczaniu rany omówionym szczegółowo w konsensusie antyseptyki z 2023 r. i w higienie rany [2, 7]. W kontekście rany debridement oznacza chirurgiczne, głębokie oczyszczanie, natomiast cleansing czy też przemywanie odnosi się do usuwania zanieczyszczeń, martwej tkanki i ciał obcych z powierzchni rany. Często obejmuje stosowanie takich technik, jak płukanie, namaczanie i irygacja, a celem oczyszczenia rany jest stworzenie optymalnego środowiska dla procesu gojenia. Na rycinie 3 przedstawiono możliwe sposoby oczyszczania łożyska rany.
Stosowanie lawaseptyków w procesie oczyszczania rany jest fundamentem strategii 4 kroków higieny rany i opiera się głownie na stosowaniu lawaseptyku z surfaktantem [2, 11]. Surfaktant to substancja obniżająca napięcie powierzchniowe powierzchni, na które działa np. powierzchni biofilmu czy zeschniętego włóknika – co ułatwia destabilizację jego struktury, ułatwiając rozluźnienie i naruszenie. Wśród surfaktantów można wymienić betainę, etyloheksyloglicerynę czy poloksamer. Lawaseptyki często zawierają w swoim składzie substancję przeciwdrobnoustrojową w małym stężeniu, np. oktenidynę, poliheksanidynę czy podchloryny (kwas podchlorawy lub podchloryn sodu). Stosowanie produktów do oczyszczania ran, czyli lawaseptyków, zajmuje kluczowe miejsce w procesie terapeutycznym i przypisuje mu się coraz większą rolą w zmniejszeniu obciążenia mikrobiologicznego w ranie, w tym w usunięciu biofilmu. Prawidłowe oczyszczenie łożyska rany jest warunkiem zastosowania antyseptyki w leczeniu ran z infekcją lub zagrożonych infekcją. Cechy lawaseptyku warte rozważenia przy wyborze przedstawiono w tabeli III.

Zarządzanie infekcją – dwutygodniowe wyzwanie w stosowaniu antyseptyków
Istniejący od 2018 r. konsensus Kramera definiuje i opisuje substancje bójcze, wskazując zasadność ich stosowania w zależności od cech rany i jej etiologii [20]. Zgodnie z IWII, EWMA i konsensusem antyseptyki Naira i wsp. z 2023 r. należy pamiętać, że substancje te należy stosować rozważnie w związku z rozprzestrzenianiem się AMR. Istnieje zgoda co do tego, że preparaty o działaniu antyseptycznym i środki przeciwdrobnoustrojowe powinny być używane po oczyszczeniu rany lawaseptykami i usunięciu z niej wszelkich zanieczyszczeń i barier, tj. martwej tkanki, włóknika, biofilmu. Nowy konsensus antyseptyki wskazuje, że antyseptyki stosowane w leczeniu ran, np. PVP-I, OCT/PE, i ewentualnie antybiotyki czy opatrunki o działaniu bójczym miejscowym powinny mieć swój określony czas stosowania [7]. Wśród ekspertów nadal trwa debata na temat najbardziej właściwego i realnego czasu leczenia infekcji w ranie. Wyzwaniem jest 14 dni terapeutycznych nazwanych przez międzynarodowych ekspertów wyzwaniem dwutygodniowym [7, 11]. Wiadomo, że wydłużony czas jest związany z podwyższonym ryzykiem rozpowszechniania się oporności na środki przeciwdrobnoustrojowe AMR, w tym oporności krzyżowej. Zaleca się zatem wdrożenie dwutygodniowego okresu, w ramach którego personel medyczny w celu opanowania infekcji powinien stosować miejscowo antyseptyki. Po 2 tygodniach pracownicy służby zdrowia powinni przeprowadzić ponowną ocenę postępu terapii oraz:
przerwać stosowanie w przypadku wyeliminowania cech infekcji,
- kontynuować stosowanie antyseptyku, jeśli stan rany się poprawia, ale wciąż obecne są objawy zakażenia (leczenie może trwać do 4 tygodni),
- w przypadku braku poprawy rozważyć alternatywny środek przeciwdrobnoustrojowy,
- ponownie ocenić chorobę podstawową.
W tabeli IV przedstawiono zalecenia i przeciwwskazania dotyczące stosowania antyseptyków.

Należy pamiętać, że preparaty o działaniu antyseptycznym nigdy nie powinny być jedyną metodą zapobiegania lub leczenia zakażeń. Są one jedynie czynnikiem wspomagającym leczenie – tak samo jak antybiotyki. Istnieją silne i coraz liczniejsze dowody, że antyseptyki mogą być przydatne w ograniczaniu rozprzestrzeniającej się antybiotykooporności AMR [4, 11]. Zgodnie z stwierdzeniem „lepiej zapobiegać niż leczyć” skuteczna antyseptyka zmniejsza ryzyko infekcji. Pomimo zawartych w konsensusie Kramera zaleceń antyseptyki nie są powszechnie stosowane w profilaktyce zakażenia miejsca operowanego, szczególnie u osób narażonych na ryzyko infekcji rany pooperacyjnej czy jej powikłania [25, 26]. Należy rozpatrzyć stosowanie produktów o szerokim i szybkim działaniu do antyseptyki szwów pooperacyjnych oraz skóry błoń śluzowych wokół rany pooperacyjnej. Należy również pochylić się nad ciszą pooperacyjną rany, czyli nad stosowaniem opatrunków specjalistycznych barierowych chroniących ranę pooperacyjną. Brak badań klinicznych oraz dowodów o silnej sile uniemożliwia w chwili obecnej aktualizację zaleceń WHO z 2018 r. dotyczących profilaktyki zakażenia miejsca operowanego.
Preparaty o działaniu antyseptycznym muszą być stosowane roztropnie, a lekarze powinni zasięgać rady konsultantów, mikrobiologów lub odpowiednich ekspertów w razie wątpliwości na którymkolwiek etapie terapii.
Substancje o działaniu przeciwdrobnoustrojowym wykorzystywane w leczeniu ran
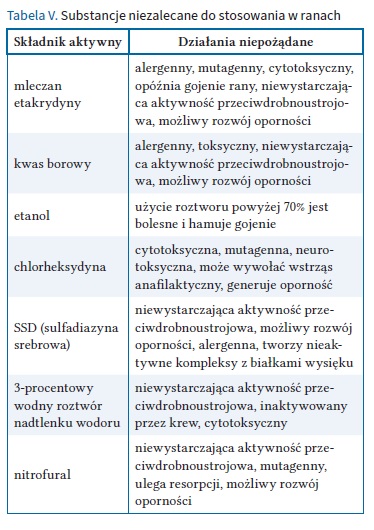
Stosowanie preparatów o działaniu antyseptycznym w ramach profilaktyki zakażenia i leczenia ran z infekcją wiąże się z wieloma wyzwaniami, m.in. z zakresem tolerancji na daną substancję, inaktywacją substancji przez materię organiczną oraz rozprzestrzenianie się oporności, w tym krzyżowej, na substancje bójcze [7, 27]. Zatem znajomość tych substancji wydaje się kluczowa w wyborze produktu. W konsensusie Kramera oraz kolejno w wytycznych PTLR, IWII i najnowszych wytycznych opracowanych przez Naira i wsp. przedstawiono charakterystykę substancji bójczych wykorzystywanych w antyseptyce ran. W każdym z tych dokumentów uwzględniono również tzw. stare antyseptyki, które nie są zalecane w terapii ran trudno gojących. Co więcej, duża ich część nie wykazuje działania bójczego. W tabeli V opisano niezalecane substancje, tzw. stare antyseptyki [11, 28].
Panel ekspertów w konsensusie antyseptyki z 2023 r. zwrócił uwagę na fakt, iż nie ma złych ani dobrych substancji w działaniu bójczym, należy je wykorzystywać zgodnie z wskazaniem i stanem rany oraz zdrowia pacjenta. Obserwowane w zależności od szerokości geograficznej różnice w stosowaniu substancji bójczych wynikają z rejestracji w danym państwie, są zależne od obowiązujących protokołów i bazują na finansowaniu systemu opieki nad raną i późniejszą kontynuacją leczenia poza murami szpitala [7]. Poniżej przedstawiono opisy najczęściej stosowanych substancji o działaniu bójczym stosowanych w profiaktyce i terapii ran, w tym ran trudno się gojących.
Oktenidyna (OCT; dichlorowodorek oktenidyny)
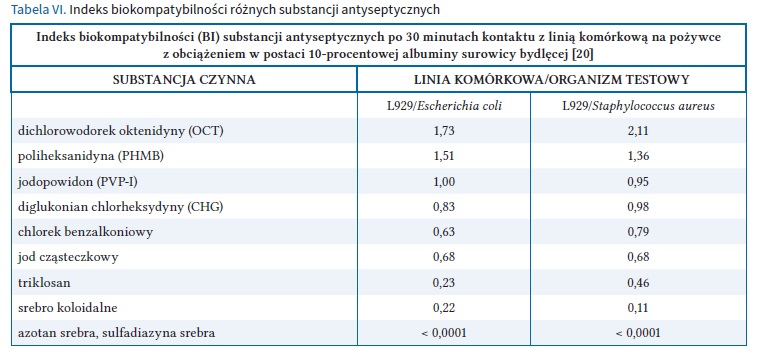
Jest powszechnie dostępną substancją o działaniu przeciwdrobnoustrojowym. Ma dwa nieoddziałujące ze sobą kationowe centra aktywne, które łatwo wiążą się z ujemnie naładowanymi zewnętrznymi warstwami drobnoustrojów, grzybów czy wirusów osłonkowych [29–31]. Po przyłączeniu OCT następuje rozluźnienie struktur osłon zewnętrznych i wyciek błony cytoplazmatycznej, a finalnie śmierć komórki drobnoustroju. Oktenidyna wykazuje szerokie spektrum bójczości wobec drobnoustrojów Gram-dodatnich oraz Gram-ujemnych, nawet tych opornych na antybiotyki oraz wobec drobnoustrojów atypowych, np. Chlamydia czy Mycoplasma oraz grzybów. Stwierdzono również działanie bójcze wobec pierwotniaków powodujących infekcje układu moczowo-płciowego Trichomonas vaginalis oraz dezaktywację wirusów głównie otoczkowych [7, 20, 29, 30]. Oktenidyna wykazuje również działanie dezaktywujące niektóre enzymy bakteryjne. W badaniach in vitro okazała się bardziej skuteczna niż chlorheksydyna wobec enzymów produkowanych przez Streptococcus mutans, biorących udział w tworzeniu płytki nazębnej [29]. Oktenidyna wykazuje szybkie działanie bójcze (30 sekund) w niskich stężeniach. Stężenie MIC dla bakterii Gram-dodatnich i Gram-ujemnych oscyluje wokół 1–4,9 μg/ml, dla grzybów z grupy Candida (Candida albicans, Candida tropicalis i Candida pseudotropicalis) 1,5–3,0 μg/ml [20, 29]. Konsensus Kramera przedstawia najlepszą skuteczność bójczą wobec drobnoustrojów w teście zawiesinowym w porównaniu z PVP-I, PHMB czy CHX (chlorheksydyną), co potwierdzają również badania Radichat i Karpińskiego [32, 33]. Oktenidyna jest stabilna i pozostaje aktywna przeciwdrobnoustrojowo w szerokim zakresie pH (1,6–12,2), co jest kluczowe szczególnie w leczeniu ran i owrzodzeń, które charakteryzują się ciągłą produkcją wysięku, a nawet krwi [29, 34, 35]. Oktenidyna ma najwyższy indeks biozgodności spośród substancji bójczych stosowanych do antyseptyki, tzn. ma szerokie spektrum działania wobec drobnoustrojów oraz niski poziom cytotoksyczności wobec fibroblastów czy keratynocytów, dzięki czemu jest substancją z wyboru do antyseptyki skóry u noworodków [7, 20, 29]. Należy zaznaczyć, iż oktenidyna nie ulega resorbcji przez skórę i błony śluzowe. Podobnie jak chlorheksydyna wykazuje przedłużony efekt bójczy, tzw. efekt rezydualny [7, 29]. Kramer i wsp. w swoim przeglądzie wskazują, że wobec biofilmu Pseudomonas aeruginosa najwiekszą skuteczność ma właśnie oktenidyna [20]. Do chwili obecnej nie wykryto ani nie wyindukowano w warunkach in vitro oporności drobnoustrojów na oktenidynę. Oktenidyna występuje w wielu produktach, które mogą mieć rejestrację leku, wyrobu medycznego czy kosmetyku, i ma swoje uzasadnione zastosowanie w antyseptyce skóry i błon śluzowych oraz antyseptyce ran, w płukaniu i czyszczeniu ran czy pielęgnacji ciała z uwzględnieniem dekontaminacji. W badaniach na modelu rany u zwierząt wykazano, że oktenidyna w połączeniu z fenoksyetanolem wspiera proces zamknięcia łożyska rany porównywalnie do płynu Ringera i nie zaburza procesu gojenia [20, 29]. Badania in vitro wskazują, że oktenidyna stymuluje produkcję cytokin i lokalnych immunomodulatorów, np. płytkowopochodnego czynnika wzrostu, co razem z aktywacją fagocytozy może wspierać proces gojenia [20, 29]. Należy pamiętać, że oktenidyna wykazuje niekorzystny wpływ na tkankę chrzęstna oraz że nie wolno wstrzykiwać lub wprowadzać produktu z oktenidyną do tkanki pod ciśnieniem, z uwzględnieniem tuneli, kieszeni bez możliwości kontroli odpływu. W każdym przypadku należy zapewnić odpowiedni odpływ z jam rany (np. drenaż, odsysacz). Wieloletnie doświadczenie i liczne protokoły badań klinicznych wskazują na synergistyczny efekt [36, 37] stosowania produktów na bazie oktenidyny i opatrunków specjalistycznych, w tym z srebrem [38]. Nie należy łączyć oktenidyny z PVP-I. Niezwykle ważne jest, by przed procedurą planowania terapii rany zapoznać się dokładnie z dokumentami rejestracyjnymi IFU czy ChPL [36].
Poliheksanidyna (PHMB)
Cząsteczka PHMB została wprowadzona do lecznictwa przez Willenegger pod koniec XX w. (1980) w Szwajcarii. Budową chemiczną przypomina chloheksydynę, jednakże różni się od niej brakiem ostatniego wiązania 4-chloroaniliny, która wykazuje silne właściwości kancerogenne dla tkanek ludzkich [20]. Poliheksanidyna wykazuje szerokie spektrum działania bójczego wobec drobnoustrojów Gram-dodatnich, Gram-ujemnych, grzybów, w tym drożdży, i niektórych wirusów oraz nie generuje oporności krzyżowej na antybiotyki [1, 7, 11, 39, 40]. W jednym z badan wykazano istotną redukcję namnażania wirusa brodawczaka ludzkiego pod wpływem stosowania PHMB, co jest tematem badań i może stać się kolejnym wskazaniem do jego użycia [20]. W małych stężeniach PHMB charakteryzuje niski poziom cytotoksyczności i wysoki indeks biozgodności [1, 4, 7, 11, 20]. W 2018 r. Kramer i wsp.wykazali wyższą skuteczność PHMB w porównaniu z sulfatiazyną, chlorheksydyną, srebrem jonowym i PVP-I. Poliheksanidyna nie uszkadza nowo odbudowanych tkanek [40]. Nie jest resorbowana do krwi i podobnie jak oktenidyna pozostaje na tkankach, zapewniając efekt rezydualny [20]. Ze względu na silne wiązanie się do komórek należy zachować podobne środki ostrożności w przypadku ran bez pewności drenażu lub odpływu jak w przypadku oktenidyny [20]. Poliheksanidyna znajduje się w wielu produktach w postaci roztworu do płukania ran, żelu. Zawarta też jest w opatrunkach. Udowodniono, że stosowanie produktów zawierających PHMB może zmniejszyć ryzyko zakażenia miejsca operowanego [20, 39]. Należy pamiętać, że PHMB wymaga dłuższego czasu kontaktu (w zależności od stężenia minimum 15 minut i więcej) w celu osiągnięcia pełnej skuteczności bakteriobójczej [7, 20, 32, 33]. Po wielu dyskusjach PHMB w małych stężeniach została uznana za niekancerogenną i w wyrobach medycznych stosowanych do płukania i nawilżania ran dostępna jest w stężeniu 0,1%, 0,02%, i 0,04% [20]. Produkty te są uznane bezpieczne. Wśród przeciwwskazań i środków ostrożności znajdują się: stosowanie na chrząstkę szklistą, płukanie jamy otrzewnej płukanie oka czy ucha oraz ciąża (główne pierwsze 4 miesiące), karmienie piersią (brak badań klinicznych) oraz ryzyko uczuleń lub reakcji anafilaktycznych [11, 20]. Badania kliniczne wskazują na istotny wpływ produktów z PHMB na proces gojenia z uwzględnieniem zapisów w dokumentach rejestracyjnych takich jak IFU [20].
Jodopowidon (PVP-I)
Może mieć postać roztworu, maści lub opatrunku. O stosowanej postaci decyduje cel terapeutyczny i wskazania opisane w dokumencie rejestracyjnym, np. ChPL, IFU. Roztwór niesterylny jodopowidonu może być stosowany zgodnie z rejestracją w postaci nierozcieńczonej do dezynfekcji ran lub w postaci rozcieńczonej w roztworze wodnym lub w alkoholu do przemywania czy płukania ran. Właściwości bakteriobójcze PVP-I wynikają z obecności wolnego, niezwiązanego jodu, który w maściach i roztworach wodnych uwalniany jest z kompleksu powidonu jodowanego jako część reakcji równoważenia [20, 41, 42]. Wolny jod reaguje jako silny środek utleniający na poziomie molekularnym, głównie z nienasyconymi kwasami tłuszczowymi i słabo utleniającymi się grupami aminokwasowymi –SH lub –OH zawartymi w enzymach i podstawowych związkach strukturalnych mikroorganizmów. Dzięki tej nieswoistej aktywności PVP-I działa bójczo na szerokie spektrum drobnoustrojów, tj. bakterie Gram-ujemne i Gram-dodatnie, prątki, grzyby (szczególnie Candida), wiele wirusów i niektóre pierwotniaków, spory bakteryjne np. Clostridium [1, 4, 7, 11, 20]. Jodopowidon w badaniach in vitro wykazał działanie hamujące na produkcję egzotoksyn bakteryjnych, a przez to skuteczne działanie zmniejszające uruchomienie prozapalnej kaskady [20, 41]. Nie zaobserwowano zjawiska oporności drobnoustrojów na PVP-I. Jodopowidon w przeciwieństwie do PHMB i OCT nie wykazuje efektu remantnego [20]. Kompleks powidonu jodowanego działa skutecznie w otoczeniu o pH z zakresu 2–7. Jodopowidon w zależności od rozcieńczenia wykazuje szybkie działanie bójcze, porównywalne do czasu wymaganego dla oktenidyny [20, 32, 33]. Działa przeciwbiofilmowo oraz penetruje biofilm dojrzały. Jodopowidon wykazuje niższy indeks biozgodności i zgodnie z doniesieniami może działać cytotoksycznie [7, 20]. Ze względu na wnikanie substancji do krwiobiegu należy rozważyć stosowanie jodopowidonu u pacjentów z chorobami tarczycy [7, 11, 20]. Zaleca się też rozwagę w stosowaniu dłużej niż przez 7 dni [20]. Wśród przeciwwskazań znajdują się nadwrażliwość lub uczulenie na jod lub którąkolwiek substancję pomocniczą, wole nadczynne, choroby tarczycy, choroba Hashimoto, opryszczkowe zapalenie skóry (choroba Duhringa), a także płukanie jamy otrzewnej. Preparaty te nie powinny być stosowane w okresie ciąży i karmienia piersią, a także u pacjentów w wieku poniżej 12 lat, przed leczeniem i po terapii radioaktywnym izotopem jodu (aż do zakończenia leczenia).
Podchloryny – kwas podchlorawy (HOCl), podchloryn sodu (NaOCl)
Produkty do leczenia ran na bazie podchlorynów zawierają w swoim składzie kwas podchlorawy lub mieszaninę podchlorynu sodu i kwasu podchlorawego. Zarejestrowane są głównie jako wyroby medyczne i mają postać płynu do płukania ran lub żelu. Występują jako produkty zawierające bardzo małe stężenie 40–50 ppm pojedynczych składników lub znacznie większe, nawet do ok. 800 ppm. Podchloryny są substancjami o wysokim potencjale utleniającym, co jest głównym mechanizmem niszczącym struktury drobnoustrojów. Komórki ludzkie nie są wrażliwe na działanie niskich stężeń rzędu 50 ppm, ponieważ są wyposażone w naturalny mechanizm detoksykacji. Jest to wynikiem naturalnego procesu produkcji HOCl podczas procesu fagocytozy. Co więcej, podchloryny są związkami niestabilnymi szczególnie w dynamicznie zmieniającym się środowisku rany, dlatego mają wysoki potencjał bezpieczeństwa i mogą być stosowane do jamy otrzewnej, płukania wyeksponowanych elementów układu kostnego, do jam ciała, oka, ucha czy wyeksponowanych elementów układu nerwowego.
Szczególne znacznie może mieć ich zastosowanie w przypadku przepłukiwania przetok bez możliwości drenażu. Związki te wykazują szerokie działanie przeciwdrobnoustrojowe, obejmujące bakterie Gram-dodatnie i Gram-ujemne, wirusy, grzyby i przetrwalniki bakteryjne [7, 11, 20, 43]. Konsensus Kramera i wsp. wskazuje działanie podchlorynów na struktury biofilmu i przypisuje im skuteczniejsze działanie niż połączenie PHMB i betainy [20, 43]. Należy jednak pamiętać o potrzebie wydłużonego czasu kontaktu (do 15 minut) na łożysku rany. Należy mieć na uwadze, że mimo szerokiego spektrum bójczego oraz szybkiego działania [7, 11, 20] podchloryny nie utrzymują się w ranie, w związku z czym nie wykazują przedłużonego działania. Niezależnie od stężenia nie wykazują efektu rezydualnego [7, 20]. Wykazano działanie przeciwzapalne, przeciwhistaminowe roztworów podchloryny sodu i kwasu podchlorawego, co wykorzystywane jest nie tylko w terapii owrzodzeń, lecz także w atopiach skórnych, np. atopowym zapaleniu skóry. Liczne badania kliniczne wskazują na wsparcie procesów gojenia z wykorzystaniem roztworu podchlorynów zarówno w ramach profilaktyki zakażenia miejsca operowanego, jak i terapii ran trudno się gojących [20].
Algorytm stosowania terapii przeciwdrobnoustrojowej AMS w dobie rosnącej antybiotykoodporności – wyzwania
Oporność na środki przeciwdrobnoustrojowe jest poważnym globalnym zagrożeniem dla zdrowia publicznego, które wg szacunków każdego roku przyczynia się do 5 mln zgonów na całym świecie (WHO, 2022). Nieprawidłowe stosowanie lub nadużywanie antybiotyków doprowadziło do rozwoju oporności bakterii AMR, dlatego istnieje pilna potrzeba poprawy procesu przepisywania antybiotyków na całym świecie. Strategia zarządzania środkami przeciwdrobnoustrojowymi (AMS) wymaga „opracowania podejścia w ramach organizacji lub całego systemu opieki zdrowotnej dotyczącego promowania i monitorowania rozsądnego stosowania środków przeciwdrobnoustrojowych w celu zachowania ich skuteczności z myślą o przyszłości” [9, 44]. Ostatecznie podejście skoncentrowane na AMS bierze pod uwagę znaczenie ochrony skuteczności antybiotyków w celu poprawy wyników leczenia pacjentów i ograniczania zakażeń powodowanych przez mikroorganizmy wielolekooporne. Powstało wiele globalnych inicjatyw mających na celu zmierzenie skuteczności tych programów w walce z AMR, a kluczowymi zidentyfikowanymi strategiami wobec AMS są:
- zwiększenie wysiłków na rzecz stworzenia skutecznych metod kontroli zakażeń, obejmujących: higienę rąk lub praktyki odkażające i dezynfekcyjne, stosowanie środków ochrony indywidualnej (ŚOI) zgodnych z lokalnym protokołem, prawidłowa utylizacja ŚOI, odpowiednie zarządzanie odpadami w tym medycznymi, prowadzenie kompleksowej dokumentacji i zarządzanie środowiskiem pacjenta,
- stworzenie spójnej bazy wiedzy i możliwości edukacyjnych dla lekarzy w zakresie skutecznego stosowania środków przeciwdrobnoustrojowych, a także zmniejszenie różnic w praktyce prowadzące do ograniczania niepewności diagnostycznej, ignorancji klinicznej, zachowań rytualnych, przyzwyczajeń, fobii klinicznych i poddawaniu się żądaniom pacjenta,
- prawidłowe postępowanie z raną bez cech infekcji, tj. przepisywanie odpowiedniego leczenia przeciwdrobnoustrojowego w sytuacji, gdy jest to konieczne i uzasadnione. Minimalizacja incydentów niepotrzebnego i nieuzasadnionego stosowania środków przeciwdrobnoustrojowych, terapii o zbyt szerokim spektrum działania bójczego, w tym stosowania antybiotyków,
- przepisywanie środków przeciwdrobnoustrojowych na odpowiedni czas kuracji, w odpowiedniej dawce, podawanych najbardziej odpowiednią drogą odpowiednio do schorzenia i stanu pacjenta (Five Rights – „Pięć zasad”; ryc. 4),
- stosowanie środka o najniższym ryzyku zdarzeń niepożądanych [1, 7, 45].

W nowym konsensusie antyseptyki zdefiniowano i podsumowano bariery towarzyszące wdrożeniu strategii zarządzania środkami przeciwdrobnoustrojowymi (AMS), które powinny być również namierzone w lokalnych ośrodkach leczenia ran. Należy pamiętać o otwartości na nowe zalecenia i doniesienia naukowe oraz edukacji personelu medycznego, pacjenta oraz jego opiekunów i rodziny. Istotnymi barierami we wdrażaniu strategii AMS, które są wyzwaniem głównie dla organów decydujących o systemie ochrony zdrowia i edukacji, są wymienione przez WHO [8]:
- deficyty wiedzy personelu medycznego w zakresie optymalnego uzasadnionego stosowania antybiotyków,
- nieefektywne zasoby i ograniczona infrastruktura dla programów wspierających strategię AMS,
- brak komunikacji i współpracy pomiędzy specjalistami różnych specjalizacji,
- zbyt kosztowne diagnostyczne badania mikrobiologiczne i limity finansowania przez płatnika,
- ograniczony dostęp do środków przeciwdrobnoustrojowych oraz brak danych na temat efektywności kosztowej,
- opór przed zmianą obecnych praktyk oraz przyzwyczajeń dotyczących przepisywania środków przeciwdrobnoustrojowych.
Ponadto liczne badania [46–48] jednoznacznie wykazały, że kształcenie podyplomowe, warsztaty edukacyjne i inne formy kształcenia i doskonalenia zawodowego w znacznym stopniu przyczyniają się do wzrostu wiedzy kadry medycznej, jednocześnie wpływając na jakość życia chorych.
Algorytm stosowania terapii przeciwdrobnoustrojowej AMS w dobie rosnącej antybiotykoodporności – postępowanie z raną bez cech lub z cechami infekcji za konsensusem antyseptyki z 2023 roku
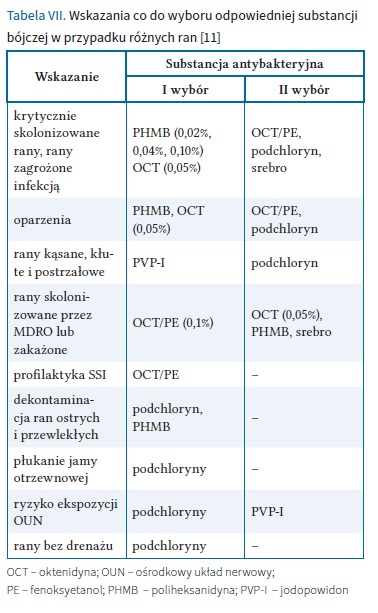
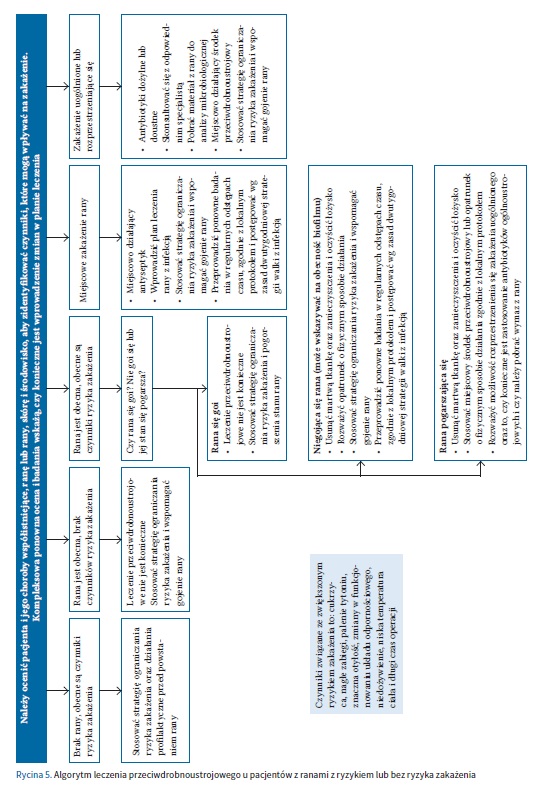
W 2020 r. PTLR przedstawiło wskazania do zastosowania poszczególnych substancji bójczych. W tabeli VII i na rycinie 5 przedstawiono aktualne wskazania oparte na etiologii i charakterze rany [11].
Podsumowanie
Postępowanie u chorego z raną musi mieć charakter kontekstowy, co w praktyce oznacza, że musi odnosić się zarówno do cech rezydualnych pacjenta, jak i miejscowych uwarunkowań rany. Wybór postępowania musi mieć również charakter zindywidualizowany, co oznacza wybór najbardziej optymalnej terapii w odniesieniu do stosunku korzyści do ryzyka określonego postępowania. Z uwagi na narastającą oporność na antybiotyki wskazane jest stosowanie substancji bójczych, które z uwagi na swoją charakterystykę mogą być z powodzeniem używane u pacjenta z raną zakażoną.
W przypadku antybiotyków podawanych systemowo uwarunkowania miejsca infekcji – zapalenie, naciek, przestrzenie płynowe, biofilm – mogą wpływać na występowanie straty dystrybucyjnej, co w praktyce oznacza brak możliwości uzyskania stabilnych parametrów decydujących o skuteczności, jak również minimalizacji presji selekcyjnej w kierunku powstawania antybiotykooporności. Stosowanie antybiotyków systemowych jako działanie niepożądane może indukować dyzbiozę, która w praktyce może stanowić jeden z elementów upośledzonego gojenia. Stosowane często w terapii fluorochinolony czy metronidazol mogą indukować wystąpienie neuropatii obwodowej, co jest niekorzystnym zjawiskiem w przypadku pacjenta z raną. Dodatkowo fluorochinolony poprzez możliwość indukowania kolagenotoksyczności dodatkowo modyfikują proces gojenia. Nie bez znaczenia dla wyboru metody postępowania jest stan kliniczny pacjenta. W szczególności u pacjenta paliatywnego, u kresu życia, zmiany w tkankach doprowadzają do zmniejszenia skuteczności antybiotykoterapii systemowej i zamiast skutecznego efektu terapeutycznego mogą indukować powikłania zmniejszające jakość życia pacjentów.
Oświadczenie
Autorzy deklarują brak konfliktu interesów.
Piśmiennictwo
- Swanson T, Ousey K, Haesler E i wsp.; International Wound Infection Institute (IWII) Wound Infection in Clinical Practice. Principles of best practice. Wounds International 2022.
- Murphy C, Atkin L, Swanson T i wsp. Defying hard-to-heal wounds with an early antibiofilm intervention strategy: wound hygiene. J Wound Care 2020; 29 (Sup3b): S1–S26. DOI: 10.12968/jowc.2020.29.Sup3b.S1.
- Murphy C, Atkin L, Hurlow J i wsp. Wound hygiene survey: awareness, implementation, barriers and outcomes. J Wound Care 2021; 30: 582–590. DOI: 10.12968/jowc.2021.30.7.582.
- Probst S, Apelqvist J, Bjarnsholt T I wsp. Antimicrobials and Non-healing Wounds: An Update. J Wound Management, 2022; 23 (3 Sup1): S1–S33.
- Antimicrobial resistance surveillance in Europe 2023 – 2021 data. Stockholm: European Centre for Disease Prevention and Control and World Health Organization; 2023.
- Mitchell BG, Shaban RZ, MacBeth D, Wood CJ, Russo PL. The burden of healthcare-associated infection in Australian hospitals: A systematic review of the literature. Infect Dis Health 2017; 22: 117–128. DOI: 10.1016/j.idh.2017.07.001
- Nair HKR, Mrozikiewicz-Rakowska B, Sanches Pinto D i wsp. International Consensus Document. Use of wound antiseptics in practice. Wounds International. Dostępne na: https://woundsinternational.com/wp-content/uploads/sites/8/2023/10/MULTI23_CD_Antiseptic_WINT_WEB.pdf.
- World Health Organization. The WHO AWaRe (Access, Watch, Reserve) antibiotic book. 2022. Dostępne na: https://www.who.int/publications/i/item/9789240062382.
- National Institute for Health and Care Excellence. Antimicrobial stewardship. 2023. Dostępne na: https://bnf.nice.org.uk/medicines-guidance/antimicrobial- stewardship/.
- European Centre for Disease Prevention and Control. Strona główna: https://www.ecdc.europa.eu/en.
- Sopata M, Jawień A, Mrozikiewicz-Rakowska B i wsp. Wytyczne postępowania miejscowego w ranach niezakażonych, zagrożonych infekcją oraz zakażonych – przegląd dostępnych substancji przeciwdrobnoustrojowych stosowanych w leczeniu ran. Zalecenia Polskiego Towarzystwa Leczenia Ran. Leczenie Ran 2020; 17: 1–21. DOI: 10.5114/LR.2020.96820.
- Wolcott RD, Hanson JD, Rees EJ, et al. Analysis of the chronic wound microbiota of 2,963 patients by 16S rDNA pyrosequencing. Wound Repair Regen 2016; 24: 163–174. doi:10.1111/wrr.12370.
- Kadam S, Shai S, Shahane A, Kaushik KS. Recent Advances in Non-Conventional Antimicrobial Approaches for Chronic Wound Biofilms: Have We Found the ‚Chink in the Armor’?. Biomedicines 2019; 7: 35. DOI: 10.3390/biomedicines7020035.
- Costerton JW, Cheng KJ, Geesey GG i wsp. Bacterial biofilms in nature and disease. Annu Rev Microbiol 1987; 41: 435–464. DOI: 10.1146/annurev.mi.41.100187.002251.
- Malka M, Krakowiecki A, Chojak M i wsp. The Pathogen Isolates in Chronic Wound Infections in Poland. Pol J Microbiol 2023; 72: 133–142. DOI: 10.33073/pjm-2023-014.
- Sopata M, Luczak J, Ciupińska M. Effect of bacteriological status on pressure ulcer healing in patients with advanced cancer. J Wound Care 2002; 11: 107–110. DOI: 10.12968/jowc.2002.11.3.26678.
- IWGDF/IDSA 2023. Guidelines on the diagnosis and treatment of foot infection in persons with diabetes. Dostępne na: https://iwgdfguidelines.org/wp-content/uploads/2023/07/IWGDF-2023-04-Infection-Guideline.pdf.
- Brock AK, Chamoun-Emanuelli AM, Howard EA i wsp. Wound swabs versus biopsies to detect methicillin resistant Staphylococcus aureus in experimental equine wounds. Vet Surg 2022; 51: 1196–1205. DOI: 10.1111/vsu.13872.
- Haalboom M, Blokhuis-Arkes MHE, Beuk RJ, et al. Culture results from wound biopsy versus wound swab: does it matter for the assessment of wound infection? Clin Microbiol Infect 2019; 25: 629.e7–629.e12. DOI: 10.1016/j.cmi.2018.08.012.
- Kramer A, Dissemond J, Kim S i wsp. Consensus on Wound Antisepsis: Update 2018. Skin Pharmacol Physiol 2018; 31: 28–58. DOI: 10.1159/000481545.
- Vejzovic D, Iftic A, Ön A i wsp. Octenidine’s Efficacy: A Matter of Interpretation or the Influence of Experimental Setups? Antibiotics (Basel) 2022; 11: 1665. DOI: 10.3390/antibiotics11111665.
- Shepherd MJ, Moore G, Wand ME i wsp. Pseudomonas aeruginosa adapts to octenidine in the laboratory and a simulated clinical setting, leading to increased tolerance to chlorhexidine and other biocides. J Hosp Infect 2018; 100: e23–e29. DOI: 10.1016/j.jhin.2018.03.037.
- Ustawa z dnia 6 września 2001 r. Prawo farmaceutyczne (Dz.U.2022.2301 t.j.).
- Rozporządzenie Parlamentu Europejskiego i Rady (UE) 2017/745 z dnia 5.04.2017 roku w sprawie wyrobów medycznych Załącznik VIII, Reguły klasyfikacji.
- Lipsky BA. Diabetic foot infections: Current treatment and delaying the ‚post-antibiotic era’. Diabetes Metab Res Rev. 2016; 32 Suppl 1: 246–253. DOI: 10.1002/dmrr.2739.
- Roberts CD, Leaper DJ, Assadian O. The Role of Topical Antiseptic Agents Within Antimicrobial Stewardship Strategies for Prevention and Treatment of Surgical Site and Chronic Open Wound Infection. Adv Wound Care (New Rochelle) 2017; 6: 63–71. DOI: 10.1089/wound.2016.0701.
- Chakraborti C, Le C, Yanofsky A. Sensitivity of superficial cultures in lower extremity wounds. J Hosp Med 2010; 5: 415–420. DOI: 10.1002/jhm.688.
- Babalska ZŁ, Korbecka-Paczkowska M, Karpiński TM. Wound Antiseptics and European Guidelines for Antiseptic Application in Wound Treatment. Pharmaceuticals (Basel) 2021; 14: 1253. DOI: 10.3390/ph14121253.
- Assadian O, Pilcher M, Antunes i wsp. Facilitating wound bed preparation: properties and clinical efficacy of octenidine and octenidine-based products in modern wound management. J Wound Care 2016; 25: S1–S28.
- Malanovic N, Buttress JA, Vejzovic D i wsp. Disruption of the Cytoplasmic Membrane Structure and Barrier Function Underlies the Potent Antiseptic Activity of Octenidine in Gram-Positive Bacteria. Appl Environ Microbiol 2022; 88: e0018022. DOI: 10.1128/aem.00180-22.
- Malanovic N, Ön A, Pabst G i wsp. Octenidine: Novel insights into the detailed killing mechanism of Gram-negative bacteria at a cellular and molecular level. Int J Antimicrob Agents 2020; 56: 106146. DOI: 10.1016/j.ijantimicag.2020.106146.
- Karpiński T, Sopata M, Mańkowski B. Skuteczność przeciwdrobnoustrojowa antyseptyków wyzwaniem w ranach trudno gojących się. Leczenie Ran 2020; 17: 88–94. DOI: https://doi.org/10.5114/lr.2020.99067.
- Radischat N, Augustin M, Herberger K i wsp. Influence of human wound exudate on the bactericidal efficacy of antiseptic agents in quantitative suspension tests on the basis of European Standards (DIN EN 13727). Int Wound J 2020; 17: 781–789. DOI: 10.1111/iwj.13336.
- Augustin M, Herberger K, Wille A, Twarock S. Impact of human wound exudate on the bactericidal efficacy of commercial antiseptic products. J Wound Care 2023; 32: 422–427. DOI: 10.12968/jowc.2023.32.7.422.
- Sopata M, Ciupińska M, Głowacka A i wsp. Effect of Octenisept antiseptic on bioburden of neoplastic ulcers in patients with advanced cancer. J Wound Care 2008; 17: 24–27. DOI: 10.12968/jowc.2008.17.1.27975.
- Cwajda-Białasik J, Mościcka P, Szewczyk MT. Antiseptics and antimicrobials for the treatment and management of chronic wounds: a systematic review of clinical trials. Postepy Dermatol Alergol 2022; 39: 141–151. DOI: 10.5114/ada.2022.113807.
- Krasowski G, Jawień A, Tukiendorf A i wsp. A comparison of an antibacterial sandwich dressing vs dressing containing silver. Wound Repair Regen 2015; 23: 525–530. DOI: 10.1111/wrr.12301.
- Sopata M, Kucharzewski M, Tomaszewska E. Antiseptic with modern wound dressings in the treatment of venous leg ulcers: clinical and microbiological aspects. J Wound Care 2016; 25: 419–426. DOI: 10.12968/jowc.2016.25.8.419.
- Barrigah-Benissan K, Ory J, Sotto A i wsp. Antiseptic Agents for Chronic Wounds: A Systematic Review. Antibiotics (Basel) 2022; 11: 350. DOI: 10.3390/antibiotics11030350.
- Rippon MG, Rogers AA, Ousey K. Polyhexamethylene biguanide and its antimicrobial role in wound healing: a narrative review. J Wound Care 2023; 32: 5–20. DOI: 10.12968/jowc.2023.32.1.5.
- Bigliardi PL, Alsagoff SAL, El-Kafrawi HY i wsp. Povidone iodine in wound healing: A review of current concepts and practices. Int J Surg 2017; 44: 260–268. DOI: 10.1016/j.ijsu.2017.06.073
- Lepelletier D, Maillard JY, Pozzetto B, Simon A. Povidone Iodine: Properties, Mechanisms of Action, and Role in Infection Control and Staphylococcus aureus Decolonization. Antimicrob Agents Chemother 2020; 64: e00682-20. DOI: 10.1128/AAC.00682-20.
- Ortega-Peña S, Hidalgo-González C, Robson MC, Krötzsch E. In vitro microbicidal, anti-biofilm and cytotoxic effects of different commercial antiseptics. Int Wound J 2017; 14: 470–479. DOI: 10.1111/iwj.12625.
- Alves PJ, Barreto RT, Barrois BM i wsp. Update on the role of antiseptics in the management of chronic wounds with critical colonisation and/or biofilm. Int Wound J 2021; 18: 342–358. DOI: 10.1111/iwj.13537.
- Stryja J, Sandy-Hodgetts K, Collier M, et al. Surgical site infection: prevention and management across health-care sectors. J Wound Care 2020; 29 (Sup2b): S1–S72. DOI: 10.12968/jowc.2020.29.Sup2b.S1.
- Głowacz J, Szwamel K. Wiedza personelu pielęgniarskiego na temat ran przewlekłych i metod ich leczenia. Pielęg Chir Angiol 2022; 16: 25–34.
- Goudy-Egger L, Dunn KS. Use of continuing education to increase nurses knowledge of chronic wound care management. J Contin Educ Nurs 2018; 49: 454–459. DOI: 10.3928/00220124-20180918-05.
- Pytlak K, Szymańska P, Skórka M, Bazaliński D. Jakość życia chorych objętych Kompleksowym Leczeniem Ran Przewlekłych. Pielęg Chir Angiol 2023; 17: 38–45.
Disclosure
The authors declare no conflict of interest.
References
- von Beckerath O, Kanya S, Gäbel G, et al. Use of maggot debridement therapy in hospitalised patients in Germany. Int Wound J 2020; 17: 10–15. DOI: 10.1111/iwj.13204.
- Probst S, Seppänen S, Gerber V, et al. EWMA document: home care – wound care. J Wound Care 2014; 23 (Suppl. 5a): S1–S44.
- Davies CE, Woolfrey G, Hogg N, et al. Maggots as a wound debridement agent for chronic venous leg ulcers under graduated compression bandages: A randomised controlled trial. Phlebology 2015; 30: 693–699. DOI: 10.1177/0268355514555386.
- Dumville JC, Worthy G, Bland JM, et al. Larval therapy for leg ulcers (VenUS II): randomized controlled trial. BMJ 2009; 338: b773. DOI: 10.1136/bmj.b773.
- Malekian A, Esmaeeli Djavid G, Akbarzadeh K, et al. Efficacy of Maggot Therapy on Staphylococcus aureus and Pseudomonas aeruginosa in Diabetic Foot Ulcers: A Randomized Controlled Trial. J Wound Ostomy Continence Nurs 2019; 46: 25–29. DOI: 10.1097/ WON.0000000000000496.
- Mudge E, Price P, Walkley N, Harding KG. A randomized controlled trial of larval therapy for the debridement of leg ulcers: results of a multicenter, randomized, controlled, open, observer blind, parallel group study [published correction appears in Wound Repair Regen 2014; 22: 290. Neal, Walkley [corrected to Walkley, Neal]]. Wound Repair Regen 2014; 22: 43–51. DOI: 10.1111/wrr.12127.
- Opletalová K, Blaizot X, Mourgeon B, et al. Maggot therapy for wound debridement: a randomized multicenter trial. Arch Dermatol 2012; 148: 432–438. DOI: 10.1001/archdermatol.2011.1895.
- Jafari A, Hosseini SV, Hemmat HJ, Khazraei H. Lucillia Sericata larval therapy in the treatment of diabetic chronic wounds. J Diabetes Metab Disord 2022; 21: 305–312. DOI: 10.1007/s40200-022-00973-w.
- Moya-López J, Costela-Ruiz V, García-Recio E, et al. Advantages of Maggot Debridement Therapy for Chronic Wounds: A Bibliographic Review. Adv Skin Wound Care 2020; 33: 515–525. DOI: 10.1097/01. ASW.0000695776.26946.68.
- Sibbald RG, Elliott JA, Persaud-Jaimangal R, et al. Wound bed preparation 2021. Adv Skin Wound Care 2021; 34: 183–195.
- Atkin L, Bućko Z, Conde Montero E, et al. Implementing TIMERS: the race against hard-to-heal wounds. J Wound Care 2019; 28 (3 Suppl. 3): 1-49.L.
- Skórka M, Bazaliński D, Gajdek M, et al. Debridement of hard-to-heel wounds provided in the home-care setting. Practical and legal possibilities. Leczenie Ran 2022; 19: 84–93. DOI: 10.5114/lr.2022.120199.
- Sherman RA. Mechanisms of maggot-induced wound healing: what do we know, and where do we go from here? Evid Based. Complement Alternat Med 2014; 2014: 592419.
- Sherman RA, Shimoda KJ. Presurgical maggot debridement of soft tissue wounds is associated with decreased rates of postoperative infection. Clin Infect Dis 2004; 39: 1067–1070. DOI: 10.1086/423806.
- Elraiyah T, Domecq JP, Prutsky G, et al. A systematic review and meta-analysis of débridement methods for chronic diabetic foot ulcers. J Vasc Surg 2016; 63 (2 Suppl): 37S–45S.e2. DOI: 10.1016/j.jvs.2015.10.002.
- Bazaliński D, Kózka M, Karnas M, Więch P. Effectiveness of Chronic Wound Debridement with the Use of Larvae of Lucilia Sericata. J Clin Med 2019; 8: 1845. DOI: 10.3390/jcm8111845.
- Tombulturk FK, Kanigur-Sultuybek G. A molecular approach to maggot debridement therapy with Lucilia sericata and its excretions/secretions in wound healing. Wound Repair Regen 2021; 29: 1051–1061. DOI: 10.1111/wrr.12961.
- Gazi U, Taylan-Ozkan A, Mumcuoglu KY. The effect of Lucilia sericata larval excretion/secretion (ES) products on cellular responses in wound healing. Med Vet Entomol 2021; 35: 257–266. DOI: 10.1111/mve.12497.
- Bazaliński D, Skórka M, Szymańska P, et al. Lucilia sericata defensins and their capacity to stimulate wound regenerative processes. A review of the literature and our own observations. Leczenie Ran 2022; 19: 94–105. DOI: 10.5114/lr.2022.120200.
- Sun X, Chen J, Zhan J, et al. Maggot debridement therapy promotes diabetic foot wound healing by up-regulating endothelial cell activity. J Diabetes Complications 2016; 30: 318–322
- Szewczyk M, Cwajda-Białasik J, Mościcka P, et al. Treatment of pressure ulcers – recommendations of the Polish Wound Management Association. Part II. Leczenie Ran. 2020; 18: 151–184. DOI: 10.5114/lr.2020.103116.
- Bazaliński D. Skuteczność terapii biologicznej z wykorzystaniem larw Lucilia sericata w leczeniu ran przewlekłych u chorych w opiece długoterminowej i paliatywnej. Wydawnictwo Uniwersytetu Rzeszowskiego, Rzeszów 2019.
- Zarchi K, Jemec GBE. The efficacy of maggot debridement therapy a review of comparative clinical trials. Int Wound J 2012; 9: 469–477.
- Sherman RA. Maggot versus conservative debridement therapy for the treatment of pressure ulcers. Wound Repair Regen 2002; 10: 208–214. DOI: 10.1046/j.1524-475x.2002.10403
- Morozov AM, Sherman RA. Survey of patients of the Tver region of Russia regarding maggots and maggot therapy. Int Wound J 2019; 16: 401–405.
- Shi E, Shofler D. Maggot debridement therapy: a systematic review. Br J Community Nurs 2014; Suppl Wound Care: S6–13.
- Tian X, Liang XM, Song GM, et al. Maggot debridement therapy for the treatment of diabetic foot ulcers: a meta-analysis. J Wound Care 2013; 22: 462–469. DOI: 10.12968/jowc.2013.22.9.462.
- Mumcuoglu KY, Davidson E, Avidan A, Gilead L. Pain related to maggot debridement therapy. J Wound Care 2012; 21: 400, 402, 404–405.

