Wytyczne
Stanowisko Polskiego Towarzystwa Leczenia Ran na temat terapii larwalnej ran
Beata Mrozikiewicz-Rakowska![]() 1, Marcin Tusiński2, Przemysław Lipiński
1, Marcin Tusiński2, Przemysław Lipiński![]() 3, Dariusz Bazaliński
3, Dariusz Bazaliński![]() 4,5, Jolanta Dynarska6, Lidia Czwakiel7, Aneta Zymon8, Bożena Mospan9, Katarzyna Malinowska10, Maciej Sopata
4,5, Jolanta Dynarska6, Lidia Czwakiel7, Aneta Zymon8, Bożena Mospan9, Katarzyna Malinowska10, Maciej Sopata![]() 11, Arkadiusz Jawień
11, Arkadiusz Jawień![]() 12,13
12,13
1 Klinika Endokrynologii, Centrum Medyczne Kształcenia Podyplomowego w Warszawie, Polska
2 Centrum Medyczne Celeris w Krakowie, Polska
3 Pracownia Leczenia Ran, ARGO Centrum Medyczne w Łodzi, Polska
4 Szpital Specjalistyczny w Brzozowie, Podkarpacki Ośrodek Onkologii, Polska
5 Instytut Nauk o Zdrowiu, Kolegium Nauk Medycznych, Uniwersytet Rzeszowski, Polska
6 Centrum Medyczne Jolanta Dynarska w Szczecinie, Polska
7 Szpital Wojewódzki im. św. Łukasza, SPZOZ w Tarnowie, Polska
8 AZ MED Centrum Leczenia Bólu i Ran w Krakowie, Polska
9 Lubuskie Centrum Diabetologii, Zielona Góra, Polska
10 0 Fundacja O!Rany, Medycyna Ran w Bydgoszczy, Polska
11 Katedra i Klinika Medycyny Paliatywnej, Hospicjum Stacjonarne Uniwersytetu Medycznego im. K. Marcinkowskiego w Poznaniu
12 Katedra i Klinika Chirurgii Naczyniowej i Angiologii, Collegium Medicum w Bydgoszczy, Uniwersytet Mikołaja Kopernika w Toruniu, Polska
13 Szpital Uniwersytecki nr 1 im. dr. A. Jurasza w Bydgoszczy, Polska
Adres do korespondencji: prof. Beata Mrozikiewicz-Rakowska, Klinika Endokrynologii, Centrum Medyczne Kształcenia Podyplomowego, ul. Marymoncka 99/103, 01-813 Warszawa, Polska e-mail: klinendo@cmkp.edu.pl
Nadesłano: 1.08.2023
Zaakceptowano: 27.09.2023
Opublikowano: 30.09.2023
LECZENIE RAN 2023; 20 (3): A89–A95
DOI: 10.60075/lr.v20i3.43
Spis treści:
Cel opracowania
Wykorzystanie terapii larwalnej rany (TLR) w procesie leczenia jest uznaną przez międzynarodowe towarzystwa naukowe oraz systemy opieki zdrowotnej wielu krajów metodą terapii miejscowej ran trudno gojących się (przewlekłych) [1, 2]. Od ponad dekady TLR jest coraz powszechniej stosowana w Polsce – zarówno w warunkach ambulatoryjnych, jak i szpitalnych.
Polskie Towarzystwo Leczenia Ran niniejszym dokumentem wspiera stosowanie tej metody przez lekarzy i pielęgniarki uprawnione do leczenia ran na podstawie odrębnych przepisów. Mając na względzie stałe podnoszenie jakości leczenia ran w naszym kraju, Towarzystwo dostrzega konieczność usystematyzowania zasad tej formy terapii.
Specyfika omawianej metody oraz specyfika samego leczenia ran powodują, że dostępna liczba badań naukowych najwyższej jakości, tj. porównawczych badań z randomizacją, jest bardzo ograniczona [3–7]. Niniejsze stanowisko powstało zatem na podstawie wyników dostępnych badań, w tym opisów przypadków, opisów serii przypadków, badań in vitro i badań z zakresu nauk podstawowych, a także doświadczenia klinicznego autorów.
Autorzy identyfikują różne obszary sporne dotyczące stosowania TLR, nieomówione w niniejszym dokumencie, co do których dostępne dowody naukowe nie pozwoliły na zajęcie jednoznacznego stanowiska. W niektórych zagadnieniach budzących kontrowersje wśród autorów, przy braku wystarczających przesłanek naukowych, przyjęto stanowisko o charakterze zachowawczym.
Opracowanie rany z wykorzystaniem larw muchy Lucilia sericata (terapia larwalna rany) jest metodą bezpieczną i łatwą do zastosowania w praktyce klinicznej w lecznictwie ambulatoryjnym i zamkniętym. Jest to szczególna forma miejscowej terapii wykorzystująca żywą postać owada w stadium larwalnym [8, 9].
Przygotowanie łożyska rany poprzez eliminację zdewitalizowanych i nekrotycznych tkanek oraz zmniejszenie obciążenia bakteryjnego jest kluczowym działaniem w celu skrócenia fazy zapalnej i stworzenia warunków do gojenia i regeneracji tkanek. Decyzja o wyborze optymalnego sposobu oczyszczania rany powinna być podejmowana z uwzględnieniem etiologii oraz stanu rany, dostępnych zasobów, jak również preferencji pacjenta [10–12].
Nazewnictwo
W piśmiennictwie anglojęzycznym najpowszechniej stosowane są terminy maggot debridement therapy (MDT) oraz larval debridement therapy (LDT) [8, 13]. W niniejszym opracowaniu proponujemy użycie polskiej nazwy „terapia larwalna rany”, w skrócie TLR. Za poprawne uważamy również takie określenia, jak „terapia z wykorzystaniem larw”, „biochirurgia z zastosowaniem larw” i „larwoterapia”.
Mechanizm działania
Terapia larwalna rany opiera się na działaniu wielokierunkowym: mechanicznym, enzymatycznym, bakteriobójczym i bakteriostatycznym, a także na zjawisku wspomagania procesu gojenia przez kontakt fizyczny larw z łożyskiem rany [13–15].
Niedojrzałe i niezdolne do rozmnażania larwy są nekrofagami. Przez okres bytowania w ranie, żywiąc się aktywnie i agresywnie martwą tkanką, którą trawią zewnątrzustrojowo, przyswajają w ciągu 24 godzin ok. 25 mg tkanki w przeliczeniu na jednego osobnika [16].
Wydzieliny produkowane przez larwy (tzw. defensyny) są substancjami białkowymi o działaniu bakteriobójczym oraz stymulującym procesy naprawcze w łożysku rany. Siła działania proteolitycznego wydalin i wydzielin, a także ich aktywność antybakteryjna, antybiofilmowa, przeciwzapalna oraz synergizm z wybranymi antybiotykami są uzależnione od liczby larw na określonym obszarze, rodzaju obecnych drobnoustrojów oraz ilości wysięku
[13, 17–20].
Bezpieczeństwo terapii i kompetencje personelu
Terapia larwalna rany jest metodą bezpieczną i obarczoną niewielkim ryzykiem wystąpienia działań niepożądanych, które zostały wymienione w dalszej części dokumentu.
Terapia larwalna rany może być prowadzona wyłącznie przez osobę posiadającą prawo wykonywania zawodu pielęgniarki lub lekarza. Pielęgniarka nieposiadająca tytułu magistra pielęgniarstwa powinna zgodnie z przepisami ukończyć kurs leczenia ran.
Formy terapii larwalnej rany
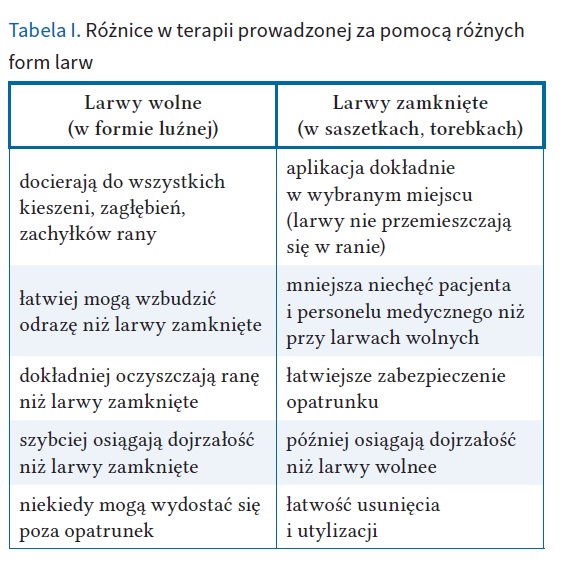
Dostępne są dwie formy przygotowania larw do stosowania w TLR: larwy wolne i larwy zamknięte. Wybór formy zastosowanej w konkretnym przypadku należy do osoby prowadzącej leczenie. Podstawowe różnice w specyfice terapii przy użyciu każdej z form przedstawiono w tabeli I [13, 14, 19, 21, 22].
Zamówienie, transport i przechowywanie
Producent zapewnia kontrolę mikrobiologiczną i gatunkową produktu. Na zamówienie przygotowuje i dostarcza larwy w liczbie i formie określonej przez osobę prowadzącą terapię. Dla larw wolnych zalecana ilość to 5–10 sztuk larw na centymetr kwadratowy rany. Larwy zamknięte zamawia się, dobierając rozmiar i liczbę torebek do rozmiaru i kształtu
rany [13, 23].
Na producencie spoczywa odpowiedzialność za dostarczenie larw gotowych do aplikacji, tj. żywych i we właściwym stadium rozwoju. Aby to osiągnąć, producent zapewnia tzw. zimny łańcuch dostaw i właściwe opakowanie w czasie transportu ze swojego laboratorium do placówki medycznej lub miejsca pobytu chorego, gdzie larwy będą aplikowane. Producent powinien zapewnić takie warunki i tempo transportu, aby określony przez niego termin ważności upływał nie wcześniej niż 24 godziny od dostarczenia larw we wskazane miejsce.
Opakowanie produktu powinno umożliwiać identyfikację partii, określać liczbę larw, datę wytworzenia i termin przydatności. Załączone materiały informacyjne powinny wyraźnie wskazywać na konieczność prowadzenia terapii wyłącznie przez osoby uprawnione do leczenia ran.
Larwy należy zaaplikować przed upływem terminu ważności określonego przez producenta, przy czym zalecane jest skrócenie okresu pomiędzy dostarczeniem larw a ich aplikacją do minimum. Za przechowywanie larw w tym okresie odpowiada osoba prowadząca terapię. Zalecane jest przechowywanie w temperaturze 4–8°C.
Bezpośrednio przed aplikacją należy potwierdzić żywotność larw na podstawie wzrokowej oceny ich ruchliwości. Jeśli istnieją wątpliwości co do żywotności larw, można powtórzyć ocenę po ogrzaniu pojemnika do temperatury pokojowej. Nie wolno aplikować larw na ranę, jeżeli pozostają jakiekolwiek wątpliwości, czy są one żywe.
Przygotowanie pacjenta [21, 22]
Należy uzyskać pisemną zgodę pacjenta lub opiekuna prawnego na zastosowanie TLR.
Przed aplikacją należy szczegółowo poinformować pacjenta i opiekuna o:
- celu zastosowania TLR oraz spodziewanych korzyściach,
- zasadach działania TLR,
- zasadach postępowania i zachowania w czasie terapii,
- przebiegu terapii, w tym o czynnościach zaleconych do wykonywania (np. zmiana opatrunku wtórnego),
- możliwych nieprzyjemnych odczuciach związanych np. z przykrym zapachem albo możliwością zaobserwowania larw, które mogą się wydostać z opatrunku,
- możliwych działaniach niepożądanych i sposobach postępowania w przypadku ich wystąpienia,
- formie komunikacji z osobą prowadzącą terapię.
Przygotowanie rany i otoczenia [13, 14, 16, 21]
W przypadku ran z dużą ilością tkanek martwiczych zalecamy przed aplikacją larw wstępne opracowanie rany z wykorzystaniem narzędzi ostrych.
Przed aplikacją należy przemyć ranę płynem obojętnym i mechanicznie oczyścić z wolnych fragmentów martwych tkanek, wysięku i włóknika (ryc. 1A).
Z uwagi na drażniący charakter wydzielanych substancji należy zabezpieczyć skórę wokół rany. W zależności od typu rany, lokalizacji i indywidualnych właściwości skóry pacjenta proponuje się w tym celu preparaty w postaci maści lub pasty z zawartością cynku, pastę stomijną albo opatrunki hydrokoloidowe (ryc. 1B).
Zasady aplikacji [13, 14, 21]
A. Dla larw wolnych
Proponujemy dwa najczęściej stosowane sposoby aplikacji larw wolnych:
1) za pomocą pipety:
Do fiolki z larwami wlać roztwór soli fizjologicznej, spłukując larwy ze ścianek i korka, tak aby opadły na dno. Następnie należy za pomocą jednorazowej sterylnej pipety Pasteura pobrać płyn z larwami i zakroplić go do rany (ryc. 2A). W jednej „gęstej” kropli znajduje się 40–50 larw. Ten rodzaj aplikacji umożliwia kontrolę nad ilością larw umieszczanych jednocześnie w kilku ranach (ryc. 2B);
2) przez wypłukanie:
Złożyć jałowy gazik włókninowy tak, aby powstała forma łódki. Do fiolki z larwami wlać roztwór soli fizjologicznej, spłukując larwy ze ścianek i korka, tak aby opadły na dno. Następnie płyn przelać powoli na uformowany gazik, odsączając larwy. Czynność wypłukiwania powtarzać do momentu zebrania całego materiału biologicznego na gaziku. Umieścić w ranie gazik, odwracając go do rany stroną z wypłukanym materiałem.
Po wprowadzeniu larw pokryć ranę kilkoma warstwami wilgotnych, jałowych gazików włókninowych. Kolejnym etapem jest nałożenie gazy na większy obszar niż rana i zabezpieczenie całości przy użyciu bandaża i plastra, w sposób uniemożliwiający zsunięcie się opatrunku w trakcie terapii. Powstaje w ten sposób opatrunek pierwotny, którego nie należy bez istotnej potrzeby zdejmować przez cały okres TLR.
Na opatrunek pierwotny należy założyć i umocować opatrunek wtórny o charakterze chłonnym, wykonany z gazy albo gotowy opatrunek wysokiej chłonności (superabsorbent).
B. Dla larw zamkniętych
Saszetki (torebki) wydobyć z fiolki transportowej narzędziem o gładkiej powierzchni, tak by nie doszło do ich przedziurawienia, a następnie założyć na przygotowane łożysko rany (ryc. 1C). Za pomocą bandaża umocować saszetki na ranie, chroniąc przed niepożądanym przemieszczeniem, nie stosując nadmiernego ucisku (ryc. 1D, E). Bandaż zabezpieczyć plastrem. Na tak wykonany opatrunek pierwotny należy założyć i umocować opatrunek wtórny o charakterze chłonnym, wykonany z gazy albo gotowy opatrunek wysokiej chłonności (superabsorbent) (ryc. 1F). Opatrunek wtórny należy również stabilnie zamocować (ryc. 1G, H).
Postępowanie w trakcie terapii larwalnej rany [13, 16, 21, 22]
Opatrunek wtórny powinien być zmieniany odpowiednio do ilości wysięku (zwykle 1–4 razy na dobę), tak aby zredukować ryzyko podrażnienia okolicy rany i zapewnić komfort choremu przez usuwanie nadmiaru cuchnącego wysięku.
Podczas zmiany opatrunku wtórnego należy nawilżać opatrunek pierwotny za pomocą wody do iniekcji lub soli fizjologicznej – zawsze w pierwszej dobie, a opcjonalnie również w trakcie kolejnych dni terapii, w zależności od ilości wysięku, tak, aby utrzymać wilgotne środowisko.
Postępowanie po zakończonej terapii
Usunięcie larw następuje w trzeciej lub czwartej dobie od aplikacji przez zdjęcie opatrunku z rany wraz z larwami wolnymi lub w torebce. Larwy wolne pozostałe w ranie należy wypłukać solą fizjologiczną i usunąć mechanicznie. Usunięty materiał należy umieścić w worku na odpady medyczne, do którego można zaaplikować alkohol izopropylowy (preparat dezynfekcyjny). Worek szczelnie zamknąć i utylizować zgodnie z procedurą przewidzianą dla odpadów
medycznych.
Ranę oraz skórę wokół należy oczyścić z wszelkich pozostałości i postępować zgodnie z dalszym planem leczenia.
Zabieg TLR można powtarzać do uzyskania zamierzonego efektu klinicznego.
Wskazania
Wskazaniem do TLR jest rana o ustalonej etiologii, bez obecności przeciwwskazań wymienionych w dalszej części dokumentu, która wymaga oczyszczenia i przygotowania do dalszych etapów leczenia [1, 8, 9, 12, 14, 15, 23, 26].
Powyższe wskazanie obejmuje:
- rany w przebiegu cukrzycowej choroby stóp o etiologii neuropatycznej, mieszanej i niedokrwiennej (po wcześniejszym leczeniu rewaskularyzacyjnym),
Zastosowanie TLR w leczeniu cukrzycowego owrzodzenia stóp skraca czas jego oczyszczania i przyspiesza wygojenie [5, 20].
- owrzodzenia goleni o etiologii żylnej, mieszanej i tętniczej (po wcześniejszym leczeniu rewaskularyzacyjnym),
Zastosowanie TLR w leczeniu owrzodzenia żylnego skraca czas jego oczyszczania, ale nie ma wpływu na czas wygojenia [3, 4, 6, 7].
- odleżyny,
Zastosowanie TLR w leczeniu odleżyny skraca czas jej oczyszczania, ale brakuje danych, czy wpływa na czas wygojenia [24].
- inne rany spełniające wyżej wymienione kryterium [13].
Terapia larwalna rany powinna być stosowana jako metoda przygotowująca ranę do dalszych etapów leczenia, np. terapii podciśnieniowej, przeszczepu skóry pośredniej grubości lub pokrycia płatem skórnym.
Przeciwwskazania [8, 9, 13, 25, 27]
- Rana o nieustalonej etiologii.
- Podejrzenie lub stwierdzenie etiologii autoimmunologicznej lub autozapalnej rany.
- Obecność nowotworu lub nacieku nowotworowego w obrębie dna lub brzegów rany.
- Rana o etiologii niedokrwiennej bez uprzedniego skutecznego leczenia rewaskularyzacyjnego.
- Anemia wymagająca przetoczenia produktów krwiopochodnych.
- Obecność suchej martwicy w ranie.
- Bezpośrednia bliskość anatomiczna dużych naczyń.
- Potencjalna komunikacja rany z jamą ciała (jama otrzewnowa, jama opłucnowa, osierdzie, śród-
piersie). - Czynne krwawienie w obrębie rany.
- Zakażenie rozprzestrzeniające się poza łożysko rany, w tym ogólnoustrojowe.
- Gorączka.
- Nieopanowane dolegliwości bólowe związane z obecnością rany przed rozpoczęciem TLR.
- Uprzednio występujące działania niepożądane w trakcie TLR.
- Brak możliwości odciążenia rany.
- Brak współpracy ze strony chorego i/lub jego opiekunów.
- Brak możliwości uzyskania świadomej zgody chorego lub opiekuna prawnego.
- Ciąża.
Przeciwwskazania względne
- Ucisk w miejscu aplikacji larw, który niesie ryzyko zniszczenia materiału biologicznego.
- Wcześniejsze spontaniczne krwawienie z rany.
- Należy każdorazowo rozważyć stosunek korzyści do ryzyka u chorych z zaburzeniami krzepnięcia oraz u chorych w trakcie terapii przeciwpłytkowej i przeciwzakrzepowej [3].
- Terapia larwalna rany nie powinna być stosowana jako jedyna metoda służąca do leczenia zakażenia rany. W przypadku zakażeń zlokalizowanych w obrębie rany TLR może być zastosowana jako metoda wspomagająca typowe leczenie antymikrobiotyczne [6, 18, 20].
- U pacjentów leczonych z użyciem kompresjoterapii zalecamy odstawienie kompresji na czas TLR, o ile nie wiąże się to z istotnym ryzykiem pogorszenia stanu rany. Podczas przerwy w kompresjoterapii właściwym postępowaniem jest elewacja kończyny [3, 4].
Działania niepożądane
Terapia larwalna rany cechuje się znikomą liczbą poważnych działań niepożądanych.
Do najczęstszych działań niepożądanych należą [7, 13, 16, 28]:
- podrażnienie i maceracja otaczającej skóry,
- zaczerwienienie skóry,
- obrzęk okolicy rany,
- ból,
- świąd.
- Do rzadziej występujących działań niepożądanych należą:
- podwyższenie temperatury lub gorączka,
- niewielkie krwawienia,
- silne krwawienie wymagające zaopatrzenia uwięzionego w martwicy naczynia krwionośnego.
Oświadczenia
Autorzy deklarują brak konfliktu interesów.
Piśmiennictwo
- von Beckerath O, Kanya S, Gäbel G, et al. Use of maggot debridement therapy in hospitalised patients in Germany. Int Wound J 2020; 17: 10–15. DOI: 10.1111/iwj.13204.
- Probst S, Seppänen S, Gerber V, et al. EWMA document: home care – wound care. J Wound Care 2014; 23 (Suppl. 5a): S1–S44.
- Davies CE, Woolfrey G, Hogg N, et al. Maggots as a wound debridement agent for chronic venous leg ulcers under graduated compression bandages: A randomised controlled trial. Phlebology 2015; 30: 693–699. DOI: 10.1177/0268355514555386.
- Dumville JC, Worthy G, Bland JM, et al. Larval therapy for leg ulcers (VenUS II): randomized controlled trial. BMJ 2009; 338: b773. DOI: 10.1136/bmj.b773.
- Malekian A, Esmaeeli Djavid G, Akbarzadeh K, et al. Efficacy of Maggot Therapy on Staphylococcus aureus and Pseudomonas aeruginosa in Diabetic Foot Ulcers: A Randomized Controlled Trial. J Wound Ostomy Continence Nurs 2019; 46: 25–29. DOI: 10.1097/ WON.0000000000000496.
- Mudge E, Price P, Walkley N, Harding KG. A randomized controlled trial of larval therapy for the debridement of leg ulcers: results of a multicenter, randomized, controlled, open, observer blind, parallel group study [published correction appears in Wound Repair Regen 2014; 22: 290. Neal, Walkley [corrected to Walkley, Neal]]. Wound Repair Regen 2014; 22: 43–51. DOI: 10.1111/wrr.12127.
- Opletalová K, Blaizot X, Mourgeon B, et al. Maggot therapy for wound debridement: a randomized multicenter trial. Arch Dermatol 2012; 148: 432–438. DOI: 10.1001/archdermatol.2011.1895.
- Jafari A, Hosseini SV, Hemmat HJ, Khazraei H. Lucillia Sericata larval therapy in the treatment of diabetic chronic wounds. J Diabetes Metab Disord 2022; 21: 305–312. DOI: 10.1007/s40200-022-00973-w.
- Moya-López J, Costela-Ruiz V, García-Recio E, et al. Advantages of Maggot Debridement Therapy for Chronic Wounds: A Bibliographic Review. Adv Skin Wound Care 2020; 33: 515–525. DOI: 10.1097/01. ASW.0000695776.26946.68.
- Sibbald RG, Elliott JA, Persaud-Jaimangal R, et al. Wound bed preparation 2021. Adv Skin Wound Care 2021; 34: 183–195.
- Atkin L, Bućko Z, Conde Montero E, et al. Implementing TIMERS: the race against hard-to-heal wounds. J Wound Care 2019; 28 (3 Suppl. 3): 1-49.L.
- Skórka M, Bazaliński D, Gajdek M, et al. Debridement of hard-to-heel wounds provided in the home-care setting. Practical and legal possibilities. Leczenie Ran 2022; 19: 84–93. DOI: 10.5114/lr.2022.120199.
- Sherman RA. Mechanisms of maggot-induced wound healing: what do we know, and where do we go from here? Evid Based. Complement Alternat Med 2014; 2014: 592419.
- Sherman RA, Shimoda KJ. Presurgical maggot debridement of soft tissue wounds is associated with decreased rates of postoperative infection. Clin Infect Dis 2004; 39: 1067–1070. DOI: 10.1086/423806.
- Elraiyah T, Domecq JP, Prutsky G, et al. A systematic review and meta-analysis of débridement methods for chronic diabetic foot ulcers. J Vasc Surg 2016; 63 (2 Suppl): 37S–45S.e2. DOI: 10.1016/j.jvs.2015.10.002.
- Bazaliński D, Kózka M, Karnas M, Więch P. Effectiveness of Chronic Wound Debridement with the Use of Larvae of Lucilia Sericata. J Clin Med 2019; 8: 1845. DOI: 10.3390/jcm8111845.
- Tombulturk FK, Kanigur-Sultuybek G. A molecular approach to maggot debridement therapy with Lucilia sericata and its excretions/secretions in wound healing. Wound Repair Regen 2021; 29: 1051–1061. DOI: 10.1111/wrr.12961.
- Gazi U, Taylan-Ozkan A, Mumcuoglu KY. The effect of Lucilia sericata larval excretion/secretion (ES) products on cellular responses in wound healing. Med Vet Entomol 2021; 35: 257–266. DOI: 10.1111/mve.12497.
- Bazaliński D, Skórka M, Szymańska P, et al. Lucilia sericata defensins and their capacity to stimulate wound regenerative processes. A review of the literature and our own observations. Leczenie Ran 2022; 19: 94–105. DOI: 10.5114/lr.2022.120200.
- Sun X, Chen J, Zhan J, et al. Maggot debridement therapy promotes diabetic foot wound healing by up-regulating endothelial cell activity. J Diabetes Complications 2016; 30: 318–322
- Szewczyk M, Cwajda-Białasik J, Mościcka P, et al. Treatment of pressure ulcers – recommendations of the Polish Wound Management Association. Part II. Leczenie Ran. 2020; 18: 151–184. DOI: 10.5114/lr.2020.103116.
- Bazaliński D. Skuteczność terapii biologicznej z wykorzystaniem larw Lucilia sericata w leczeniu ran przewlekłych u chorych w opiece długoterminowej i paliatywnej. Wydawnictwo Uniwersytetu Rzeszowskiego, Rzeszów 2019.
- Zarchi K, Jemec GBE. The efficacy of maggot debridement therapy a review of comparative clinical trials. Int Wound J 2012; 9: 469–477.
- Sherman RA. Maggot versus conservative debridement therapy for the treatment of pressure ulcers. Wound Repair Regen 2002; 10: 208–214. DOI: 10.1046/j.1524-475x.2002.10403
- Morozov AM, Sherman RA. Survey of patients of the Tver region of Russia regarding maggots and maggot therapy. Int Wound J 2019; 16: 401–405.
- Shi E, Shofler D. Maggot debridement therapy: a systematic review. Br J Community Nurs 2014; Suppl Wound Care: S6–13.
- Tian X, Liang XM, Song GM, et al. Maggot debridement therapy for the treatment of diabetic foot ulcers: a meta-analysis. J Wound Care 2013; 22: 462–469. DOI: 10.12968/jowc.2013.22.9.462.
- Mumcuoglu KY, Davidson E, Avidan A, Gilead L. Pain related to maggot debridement therapy. J Wound Care 2012; 21: 400, 402, 404–405.

