Artykuł oryginalny | Original paper
Analiza flory mikrobiologicznej owrzodzeń kończyn dolnych u pacjentów hospitalizowanych na Oddziale Dermatologicznym Wojewódzkiego Szpitala Zespolonego w Elblągu w roku 2022
Analysis of the microbial flora of lower limb ulcers in patients hospitalized in the Department of Dermatology of the Provincial Integrated Hospital in Elbląg in 2022
Monika Leończyk-Spórna![]() 1, Dominika Czarnecka1, Anna Sobieszek-Kundro
1, Dominika Czarnecka1, Anna Sobieszek-Kundro![]() 1, Halina Serafin2, Tomasz Romanowski1
1, Halina Serafin2, Tomasz Romanowski1
1 Oddział Dermatologiczny, Wojewódzki Szpital Zespolony w Elblągu, Polska
2 Medyczne Laboratorium Mikrobiologiczne – Laboratorium Bakteriologiczne w Elblągu, Polska
Adres do korespondencji: Monika Leończyk-Spórna, Oddział Dermatologiczny, Wojewódzki Szpital Zespolony w Elblągu, ul. Królewiecka 146, 82-300 Elbląg, e-mail: lek.mleonczyksporna@gmail.com
Nadesłano: 2.06.2023
Zaakceptowano: 15.09.2023
Opublikowano: 30.09.2023
LECZENIE RAN 2023; 20 (3): 96–102
DOI: 10.60075/lr.v20i3.44
Streszczenie
Wprowadzenie: Owrzodzenie (łac. ulcus) to wykwit wtórny powstały w procesie patologicznym. Jest rodzajem uszkodzenia skóry sięgającego w głąb skóry właściwej. Można wyróżnić wiele czynników etiologicznych powstawania owrzodzeń. Uznaje się, że połowa z nich występuje w przebiegu przewlekłej niewydolności żylnej. Pacjenci z owrzodzeniami kończyn dolnych stanowią istotny odsetek chorych hospitalizowanych na oddziałach dermatologicznych.
Cel pracy: Analiza ilościowego rozkładu patogenów wyhodowanych z wymazów owrzodzeń kończyn dolnych pacjentów Oddziału Dermatologicznego Wojewódzkiego Szpitala Zespolonego w Elblągu w 2022 r.
Materiał i metody: W przedstawionej pracy przeanalizowano 51 wymazów pobranych z owrzodzeń kończyn dolnych u pacjentów hospitalizowanych na Oddziale Dermatologicznym Wojewódzkiego Szpitala Zespolonego w Elblągu w 2022 r. Materiał do badania mikrobiologicznego pobierano do 24 godzin od przyjęcia do szpitala. Różnicowanie drobnoustrojów pod względem gatunku przeprowadzano za pomocą firmowych podłoży namnażająco-różnicujących oraz systemów automatycznych z panelami ID GP, ID GN (Vitek 2).
Wyniki: Łączna liczba drobnoustrojów wyhodowanych z wymazów pobranych z owrzodzeń kończyn dolnych wyniosła 143. Najczęściej izolowano następujące patogeny: Staphylococcus aureus, Pseudomonas aeruginosa, Enterobacter cloacae complex, Enterococcus faecalis i Klebsiella oxytoca. Analizowaną florę bakteryjną przyporządkowano do trzech grup: pałeczki, ziarenkowce oraz bakterie beztlenowe. Dokonano również podziału na bakterie Gram-dodatnie i Gram-ujemne.
Wnioski: Pacjenci z owrzodzeniami kończyn dolnych wymagają wielospecjalistycznego podejścia i długotrwałej opieki ze względu na przewlekły charakter zmian oraz trudność w gojeniu. To częsty powód zgłaszania się chorych do poradni, jak również szpitali. Długo utrzymujące się owrzodzenia są zasiedlane przez różne drobnoustroje. Znajomość flory mikrobiologicznej owrzodzenia jest istotna w podejmowaniu decyzji terapeutycznych.
Słowa kluczowe: flora bakteryjna, owrzodzenia żylne, gojenie owrzodzeń.
Abstract
Introduction: Ulceration (lat. ulcus) is a secondary process eruption in a pathological process. It is a type of skin extending deep into the skin. Many etiological factors can be used and can be introduced. It is believed that the south of them is in the course of the southern venous energy. Patients with ulcerations of the lower limbs provide the input of patients hospitalized in dermatological departments.
Aim of the study: Analysis of the quantitative distribution of pathogens cultured from ulceration swabs of patients of the dermatological wards of the Provincial Integrated Hospital in Elbląg in 2022.
Material and methods: Analysis of the quantitative distribution of pathogens cultured from ulceration swabs of patients of the dermatological wards of the Provincial Integrated Hospital in Elbląg in 2022.
Results: Total number of beneficial cultured from swab samples taken from elevated leg ulcers 143, isolated for Staphylococcus aureus, Pseudomonas aeruginosa, Enterobacter cloacae complex, Enterococcus faecalis and Klebsiella oxytoca. The analysed bacterial flora was assigned to three groups: bacilli, cocci and anaerobic bacteria. Dissemination to Gram-positive and Gram-negative bacteria was
also made.
Conclusions: Patients with lower limb ulcers require multidisciplinary action and additional help due to the chronic nature of the lesions and the difficulty in healing. To give medicine to the sick to clinics as well as hospitals. Long-lasting ulcers are inhabited by various good ones. Knowledge of the microbial flora of the ulcer is helpful in making a therapeutic decision.
Key words: bacterial flora, ulcer healing, venous ulcers.
Wprowadzenie
Owrzodzenie (łac. ulcus) to wykwit wtórny, który powstał w procesie patologicznym. Ma charakter uszkodzenia obejmującego naskórek i skórę właściwą. Czasami doprowadza także do destrukcji głębiej położonych tkanek. Po wygojeniu pozostawia bliznę. Cechy owrzodzeń, które należy uwzględnić podczas badania fizykalnego to umiejscowienie, liczba, kształt, rozmiar, głębokość, dno, widoczność innych struktur, brzegi, a także skórę otaczającą [1, 2].
Owrzodzenia najczęściej są zlokalizowane w obrębie kończyn dolnych. W Europie występują u około 1% dorosłych. Powstają głównie na tle przewlekłej niewydolności żylnej, miażdżycy oraz cukrzycy. Ze względu na starzenie się społeczeństwa coraz więcej pacjentów z owrzodzeniami kończyn dolnych zgłasza się do poradni specjalistycznych, jak również szpitali. To istotny problem współczesnej medycyny, który znacznie obniża jakość życia pacjentów. Proces gojenia owrzodzeń jest przewlekły i trwa od kilku miesięcy do kilku, a nawet kilkunastu lat. Leczenie jest długotrwałe oraz wymaga interdyscyplinarnego podejścia [3].
Owrzodzenia kończyn dolnych stanowią częstą przyczynę hospitalizacji na oddziałach dermatologicznych. Są one głównie wynikiem przewlekłej niewydolności żylnej. Skład flory mikrobiologicznej hodowanej z owrzodzeń ma znaczenie w podejmowaniu decyzji terapeutycznych.
Cel pracy
Celem pracy jest analiza ilościowa flory mikrobiologicznej kolonizującej owrzodzenia kończyn dolnych pacjentów hospitalizowanych na Oddziale Dermatologicznym Wojewódzkiego Szpitala Zespolonego w Elblągu w 2022 r. Owrzodzenia żylne stanowią istotny problem zdrowotny i mają negatywny wpływ na jakość życia pacjentów, a dla personelu medycznego stanowią niejednokrotnie wyzwanie kliniczne [4].
Materiał i metody
W przedstawionej pracy przeanalizowano 51 wymazów z owrzodzeń kończyn dolnych u 39 pacjentów hospitalizowanych na Oddziale Dermatologicznym Wojewódzkiego Szpitala Zespolonego w Elblągu w 2022 r. (u 12 pacjentów wykonano po 2 wymazy). U większości chorych były to owrzodzenia na tle przewlekłej niewydolności żylnej.
Materiał z owrzodzeń pobierano do 24 godzin od przyjęcia do szpitala. Przy użyciu jałowych gazików i 0,9-procentowego roztworu Natrium Chloratum (chlorku sodu) usunięto zmiany martwicze, wydzielinę oraz resztki opatrunku. Wymazówką, zwilżoną jałowym roztworem chlorku sodu, pobrano materiał z dna owrzodzenia, a następnie umieszczono w szczelnie zamkniętym podłożu transportowym. Materiał przekazywano do badania mikrobiologicznego prowadzonego przez Medyczne Laboratorium Mikrobiologiczne – Laboratorium Bakteriologiczne w Elblągu.
Różnicowanie drobnoustrojów pod względem gatunku przeprowadzano na podstawie firmowych podłoży namnażająco-różnicujących (bioMerieux, Polska):
- Columbia Agar z 5% dodatkiem odwłóknionej krwi baraniej – stosowane do izolacji bakterii tlenowych i beztlenowych,
- CPS chromagar – do izolacji bakterii tlenowych,
- SNVS (neomycyna, wankomycyna, krew barania) – do izolacji bakterii beztlenowych,
- podłoże McConkeya – do izolacji drobnoustrojów Gram-ujemnych (bakterie tlenowe),
- Chromagar Candida,
- Schaedler Bulion (najczulsze) – do izolacji bakterii tlenowych i beztlenowych [4, 5].
Identyfikację drobnoustrojów przeprowadzano na podstawie firmowych (bioMerieux, Polska) systemów automatycznych, używając paneli ID GP, ID GN (Vitek 2).
Wyniki
Wykonano 51 wymazów z owrzodzeń kończyn dolnych od 39 pacjentów hospitalizowanych w Oddziale Dermatologicznym Wojewódzkiego Szpitala Zespolonego w Elblągu w roku 2022 (z czego u 12 pacjentów wykonano po 2 wymazy). Pobrany materiał oceniano mikrobiologicznie. Łączna liczba wyhodowanych drobnoustrojów wyniosła 143. Najczęściej hodowano następujące patogeny: Staphylococcus aureus (21,7%), Pseudomonas aeruginosa (11,9%), Enterobacter cloacae complex (8,4%), Enterococcus faecalis (6,3%) i Klebsiella oxytoca (6,3%) (tab. I, ryc. 1).
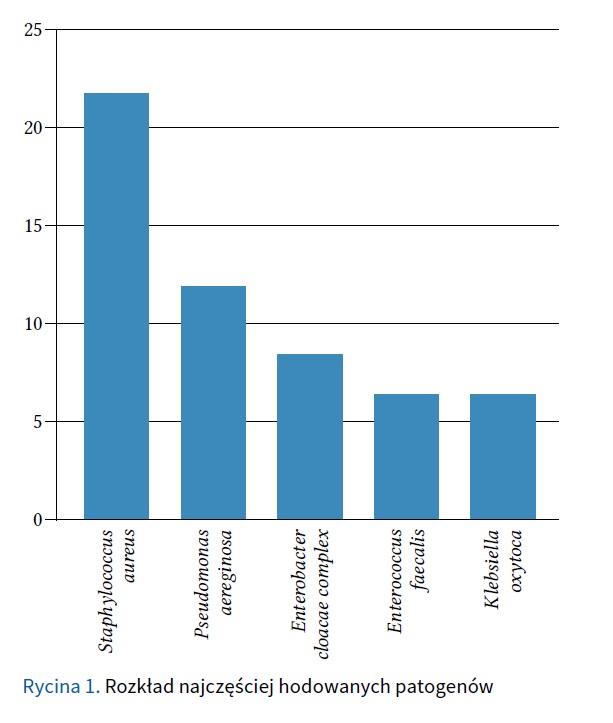
Analizę flory bakteryjnej prowadzono w trzech grupach, do których przyporządkowano wyhodowane szczepy bakteryjne (ryc. 3–5). Wyróżniono grupę pałeczek, ziarenkowców i bakterii beztlenowych. Grupę I podzielono na bakterie fermentujące i niefermentujące, zaś grupę II na gronkowce, paciorkowce β-hemolizujące i enterokoki, szeregując je od najczęściej występujących. Do III grupy zaliczono bakterie beztlenowe (tab. II, ryc. 2). Główną pałeczką fermentującą zasiedlającą owrzodzenia kończyn dolnych była Enterobacter cloacae complex, natomiast niefermentującą Pseudomonas aeruginosa. Staphyloccoccus aureus to najczęściej występujący gronkowiec. Paciorkowcem β-hemolizującym, który przede wszystkim izolowano z wymazów, był Streptococcus agalactiae, a enterokokiem Enterococcus feacalis. Wśród bakterii beztlenowych głównie stwierdzono: Bacteroides fragilis, Bacteroides thetaiotaomicron, Prevotella disiens, Prevotella oralis. W tabeli III przedstawiono podział na bakterie Gram-dodatnie i Gram-ujemne. Najczęstszą bakterią Gram-dodatnią był Staphylococcus aureus, a Gram-ujemną Pseudomonas aeruginosa.
Omówienie
Owrzodzenie jest wykwitem wtórnym, powstałym w wyniku uszkodzenia całej grubości skóry. Może obejmować także tkanki położone głębiej. Nie ma tendencji do samoistnego gojenia i ostatecznie prowadzi do powstania blizny.
Istotny problem kliniczny stanowią owrzodzenia kończyn dolnych. Mają z nimi do czynienia lekarze różnych specjalizacji, m.in. dermatolodzy, chirurdzy, diabetolodzy, lekarze medycyny rodzinnej oraz personel pielęgniarski. Schorzenie to dotyczy około 1% populacji osób dorosłych, stanowiąc przyczynę obniżonej jakości życia i znacznych kosztów opieki medycznej [6, 7]. W związku ze starzeniem się społeczeństwa wzrasta liczba chorych z owrzodzeniami. W większości przypadków owrzodzenia powstają na tle przewlekłej niewydolności żylnej. Steven Bowers i wsp. twierdzą, że owrzodzenia kończyn dolnych najczęściej obejmują owrzodzenia tętnicze, cukrzycowe i żylne, co potwierdzają obserwacje własne na Oddziale Dermatologicznym Wojewódzkiego Szpitala Zespolonego w Elblągu [8].
U podłoża owrzodzeń żylnych leżą zmiany patologiczne, immunologiczne oraz biochemiczne w łożysku żylnym, a także w mikrokrążeniu. Powstają one wskutek zaburzenia odpływu krwi z żył kończyn dolnych, niewydolności zastawek i rozwijającego się nadciśnienia żylnego. Znaczenie ma również toczący się proces zapalny [7, 9].
Rozpoznanie przewlekłej niewydolności żylnej ustala się na podstawie badania podmiotowego, przedmiotowego oraz wyników badań obrazujących układ naczyniowy. Bardzo często pierwsze objawy kliniczne tego schorzenia manifestują się zmianami skórnymi. Do cech dermatologicznych związanych z przewlekłą niewydolnością żylną zalicza się teleangiektazje, obrzęki, żyły siateczkowate, żylaki, włóknienie skóry i tkanki podskórnej (lipodermatosclerosis), owrzodzenia, przebarwienia skóry, zmiany wypryskowe, zanik biały (atrophie blanche), co potwierdza praca Millana. Owrzodzenia żylne najczęściej zlokalizowane są w ⅓ dystalnej, przyśrodkowej powierzchni goleni. Autor ponadto do zobrazowania deformacji goleni używa określenia „odwrócona butelka od szampana” [6]. W pracy pt. Chronic wounds: evaluation and management autorstwa Bowersa i Franca podano cechy owrzodzeń, które należy uwzględnić podczas badania przedmiotowego. Należą do nich umiejscowienie, liczba, kształt, rozmiar, głębokość, dno, widoczność innych struktur, brzegi, a także skóra otaczająca [10].
Na przebieg gojenia owrzodzeń wpływa wiele czynników, zarówno egzogennych, jak i endogennych. Jednym z nich jest kolonizacja powierzchni owrzodzenia przez różne drobnoustroje. Nie należy zapominać, iż skóra jest zasiedlana przez mikroorganizmy, które stanowią barierę biofizyczną chroniącą przed patogenami. W mikrobiocie dominują bakterie należące do typów Actinobacteria, Firmicutes, Proteobacteria i Bacteroidetes, głównie z rodzajów Propionibacterium sp., Staphylococcus sp., Micrococcus sp., Corynebacterium sp. i Acinetobacter sp., a także grzyby należące do rodzaju Malassezia. Gruczoły łojowe są zdominowane przez lipofilne gatunki z rodzaju Propionibacterium. W wilgotnym środowisku (np. powierzchnia podeszwowa stopy) bytują bakterie Staphylococcus sp. oraz Corynebacterium sp. Zaburzenie równowagi mikrobiomu skóry wraz z czynnikami ryzyka może prowadzić do rozwoju zakażenia w obrębie skóry i tkanki podskórnej [11, 12]. W badaniu autorstwa Byrda stwierdzono, że rodzaj zasiedlających skórę drobnoustrojów zależy przede wszystkim od lokalizacji, a dokładniej związku z mikrośrodowiskiem wilgotnym, suchym albo łojowym. W środowiskach łojowych dominowały lipofilne gatunki Propionibacterium, natomiast bakterie rozwijające się w środowiskach wilgotnych to Staphylococcus sp. i Corynebacterium sp. Praca wspomnianego autora potwierdziła również obserwacje dokonane na Oddziale Dermatologicznym Wojewódzkiego Szpitala Zespolonego w Elblągu, że płytkie owrzodzenia wiążą się z większą liczebnością Staphylococcus sp., zwłaszcza Staphylococcus aureus [13].
Owrzodzenia często zasiedlane są przez liczne mikroorganizmy, które nie powodują objawów zapalenia. W wyniku namnażania się drobnoustrojów może dojść do kolonizacji krytycznej i rozwoju zakażenia. Towarzyszą temu charakterystyczne objawy, takie jak: zwiększanie się dolegliwości bólowych i wysięku, zaburzenia procesu gojenia, widoczne cechy zapalenia w otaczających tkankach oraz krwawienie z ziarniny. Dane z piśmiennictwa wskazują, że do najczęstszych bakterii tlenowych izolowanych z owrzodzeń należą: Staphylococcus aureus, w tym szczepy lekooporne, np. metycylinooporny gronkowiec złocisty (methicillin-resistant Staphylococcus aureus – MRSA), gronkowce koagulazo-ujemne, paciorkowce β-hemolizujące (np. Streptococcus pyogenes), Enterococcus sp. (głównie Enterococcus faecalis), Corynebacterium sp., Escherichia coli, Klebsiella sp., Enterobacter sp., Proteus sp. i Pseudomonas aeruginosa [14]. Coraz częściej wykrywane są również Acinetobacter sp. oraz Stenotrophomonas maltophilia. Istotnym czynnikiem patogennym są również grzyby, głównie z rodzaju Candida [15, 16].
Niepowodzenie w leczeniu zakażeń jest związane między innymi ze zdolnością bakterii do tworzenia biofilmu, który jest uważany za główny czynnik wirulencji. Drobnoustroje wytwarzają pozakomórkową substancję polisacharydową – macierz zewnątrzkomórkową. Chroni ona patogeny przed niekorzystnymi czynnikami środowiska, w tym przed penetracją i działaniem związków przeciwdrobnoustrojowych oraz przed skuteczną obroną układu immunologicznego gospodarza. Macierz zewnątrzkomórkowa uniemożliwia dyfuzję stosowanych preparatów miejscowych w głąb biofilmu. Nie należy jednak stosować ogólnej antybiotykoterapii rutynowo czy profilaktycznie. Systemowe leczenie przeciwbakteryjne zaleca się tylko w uzasadnionych przypadkach. Wskazaniem do jego wdrożenia jest współistnienie zapalenia skóry i tkanki podskórnej oraz występowanie uogólnionych objawów zakażenia, co potwierdza praca autorstwa Narbutt i wsp. [17]. Nadużywanie antybiotyków, a także ich nieprawidłowe stosowanie prowadzi do wzrostu oporności [18, 19].
Diagnostyka mikrobiologiczna stanowi nieodzowny element prawidłowego procesu leczenia. Pobranie materiału do badania zawsze powinno być poprzedzone oczyszczeniem owrzodzeń. Aspiraty i fragmenty tkanek są bardziej miarodajne niż powierzchowne wymazy. Ocena bakteriologiczna umożliwia ustalenie wzorów lekowrażliwości patogenów, a także charakterystyki oporności, co skutkuje wyborem jak najlepszej opcji terapeutycznej dla pacjenta. Dodatni wynik badania bakteriologicznego nie jest równoznaczny z rozpoznaniem zakażenia – o ustaleniu rozpoznania zawsze decyduje obraz kliniczny [5, 17, 20, 21].
W przedstawionej pracy przeanalizowano 51 wymazów pobranych z owrzodzeń kończyn dolnych pacjentów hospitalizowanych na Oddziale Dermatologicznym Wojewódzkiego Szpitala Zespolonego w Elblągu w 2022 r. Najczęściej izolowaną bakterią był Staphylococcus aureus, kolejne to Pseudomonas aeruginosa, Enterobacter cloacae complex, Enterococcus faecalis i Klebsiella oxytoca. Wyniki te odpowiadają innym opracowaniom dostępnym w piśmiennictwie. Obserwowane częstsze izolacje bakterii Gram-ujemnych wiążą się prawdopodobnie z hospitalizacjami chorych z owrzodzeniami i nabywaniem przez nich flory szpitalnej oraz jej antagonistycznego działania w stosunku do flory pierwotnie kolonizującej owrzodzenia.
Głównym wykrywanym drobnoustrojem w owrzodzeniach kończyn dolnych był Staphylococcus aureus. To najczęstszy patogen szpitalny i pozaszpitalny. Jest najbardziej patogenną bakterią z grupy gronkowców, przede wszystkim z powodu wydzielania toksyn. Stanowi poważny problemem u pacjentów hospitalizowanych w oddziałach dermatologicznych z przewlekłymi chorobami skóry, takimi jak atopowe zapalenie skóry, pęcherzowe oddzielanie się naskórka, liszajec zakaźny, stopa cukrzycowa czy owrzodzenia żylne [14, 22]. Wraz z bakterią Pseudomonas aeruginosa stanowią najczęściej izolowane bakterie z przewlekłych owrzodzeń, co również potwierdziła przeprowadzona przez nas analiza. Koinfekcja Staphylococcus aureus i Pseudomonas aeruginosa jest bardziej zjadliwa niż infekcja pojedyncza, wykazując zarówno wrodzoną, jak i nabytą oporność na antybiotyki. Sprawia to, że leczenie infekcji jest prawdziwym wyzwaniem, szczególnie u pacjentów z chorobami współistniejącymi. W związku z tym prawidłowe i szybkie zastosowanie terapii wymaga szczegółowej znajomości zasiedlającej owrzodzenia flory mikrobiologicznej. Jest to niezbędny warunek w doborze odpowiedniego leczenia farmakologicznego i zmniejszenia objawów [23, 24].
Wnioski
Ze względu na przewlekły charakter owrzodzenia kończyn dolnych kolonizowane są przez różne drobnoustroje. Przeprowadzona w pracy analiza była zgodna z opisywanymi w literaturze najczęstszymi bakteriami zasiedlającymi owrzodzenia, a mianowicie: Staphylococcus aureus, Pseudomonas aeruginosa oraz bakterie z rodzaju Enterobacter, Enterococcus i Klebsiella.
Owrzodzenia skóry upośledzają naturalną obronę skóry i prowadzą do powstawania blizn oraz słabego ukrwienia, co dodatkowo skutkuje obniżeniem odporności miejscowej. Co więcej, powierzchnia owrzodzenia staje się idealnym miejscem do namnażania bakterii. Może to doprowadzić do rozwinięcia się miejscowej, a następnie uogólnionej infekcji. Skład flory mikrobiologicznej hodowanej z owrzodzeń ma znaczenie w podejmowaniu decyzji terapeutycznych. Wpływa również na kontrolę zakażeń owrzodzeń skóry, przyczynia się do zmniejszenia rozprzestrzeniania się infekcji, przyspieszenia gojenia oraz ukierunkowania w prawidłowym stosowaniu antybiotyków.
Oświadczenie
Autorzy deklarują brak konfliktu interesów.
Piśmiennictwo
- Zalewska-Janowska A, Błaszczyk H. Dermatologia w gabinecie lekarza podstawowej opieki zdrowotnej. Wyd. Lek. PZWL, Warszawa 2023.
- Nowicki RJ, Majewski S. Dermatologia i choroby przenoszone drogą płciową. Wyd. Lek. PZWL, Warszawa, 2023.
- Krasowski G, Kruk M. Leczenie odleżyn i ran przewlekłych. Wyd. Lek. PZWL, Warszawa, 2018.
- Nelson EA, Adderley U. Venous leg ulcers. BMJ Clin Evid 2016; 2016: 1902.
- Sopata M, Jawień A, Mrozikiewicz-Rakowska B i wsp. Wytyczne postępowania miejscowego w ranach niezakażonych, zagrożonych infekcją oraz zakażonych – przegląd dostępnych substancji przeciwdrobnoustrojowych stosowanych w leczeniu ran. Zalecenia Polskiego Towarzystwa Leczenia Ran. Leczenie Ran 2020; 17: 1–21. DOI: https://doi.org/10.5114/lr.2020.96820.
- Bonkemeyer Millan S, Gan R, Townsend PE. Venous Ulcers: Diagnosis and Treatment. Am Fam Physician 2019; 100: 298–305.
- Brajesh K. Lal. Venous ulcers of the lower extremity: Definition, epidemiology, and economic and social burdens. Semin Vasc Surg 2015; 28: 3–5. DOI: https://doi.org/10.1053/j.semvascsurg.2015.05.002
- Rudnicka L, Olszewska M, Rakowska A, Sar-Pomian M. Współczesna dermatologia 1. Wyd. Lek. PZWL, Warszawa, 2022.
- Narbutt J, Bowszyc-Dmochowska M, Kapińska-Mrowiecka M i wsp. Przewlekła niewydolność żylna – epidemiologia, klasyfikacja i obraz kliniczny. Rekomendacje diagnostyczno-terapeutyczne Polskiego Towarzystwa Dermatologicznego. Część I. Dermatol Rev/Przegl Dermatol 2018; 105: 473–485.
- Bowers S, Franco E. Chronic Wounds: Evaluation and Management. Am Fam Physician 2020; 101: 159–166.
- Kaszuba A., Szepietowski J., Adamski Z.: Dermatologia geriatryczna. Tom II. Czelej, Lublin, 2016.
- Grice EA, Dawson TL Jr. Host-microbe interactions: Malassezia and human skin. Curr Opin Microbiol 2017; 40: 81–87. DOI: 10.1016/j.mib.2017.10.024.
- Byrd AL, Belkaid Y, Segre JA. The human skin microbiome. Nat Rev Microbiol 2018; 16: 143–155. DOI: 10.1038/nrmicro.2017.157.
- Huitema L, Phillips T, Alexeev V i wsp. Intracellular escape strategies of Staphylococcus aureus in persistent cutaneous infections. Exp Dermatol 2021; 30: 1428–1439. DOI: 10.1111/exd.14235.
- Nieckula M, Fecko-Gałowicz K, Adamczuk J, Girzelska J. Opatrunki specjalistyczne stosowane w leczeniu owrzodzeń podudzi. Państwo i Społeczeństwo 2019; 19: 115–127. DOI: 10.34697/2451-0858-pis-2019-4-007.
- Musthaq S, Mazuy A, Jakus J. The microbiome in dermatology. Clin Dermatol 2018; 36: 390–398. DOI: 10.1016/j.clindermatol.2018.03.012.
- Narbutt J. Najczęstsze dermatozy w praktyce lekarza rodzinnego. Edra Urban & Partner, Wrocław, 2019.
- Narbutt J, Bowszyc-Dmochowska M, Kapińska-Mrowiecka M i wsp. Przewlekła niewydolność żylna – patogeneza, diagnostyka i leczenie farmakologiczne. Rekomendacje diagnostyczno-terapeutyczne Polskiego Towarzystwa Dermatologicznego. Część II. Dermatol Rev/Przegl Dermatol 2018; 105: 486–497.
- Narbutt J. Choroby skóry u pacjentów w podeszłym wieku w praktyce lekarza rodzinnego. Edra Urban & Partner, Wrocław 2023.
- Dissemond J. Chronisches Ulcus cruris. Hautarzt 2017; 68: 614–620. DOI: 10.1007/s00105-017-4010-8.
- Barnard E, Li H. Shaping of cutaneous function by encounters with commensals. J Physiol 2017; 595: 437–450. DOI: 10.1113/JP271638.
- Yang H, Wang WS, Tan Y i wsp. Investigation and analysis of the characteristics and drug sensitivity of bacteria in skin ulcer infections. Chin J Traumatol 2017; 20: 194–197. DOI: 10.1016/j.cjtee.2016.09.005.
- Serra R, Grande R, Butrico L i wsp. Chronic wound infections: the role of Pseudomonas aeruginosa and Staphylococcus aureus. Expert Rev Anti Infect Ther 2015; 13: 605–613. DOI: https://doi.org/10.1586/14787210.2015.1023291.
- Shettigar K, Murali TS. Virulence factors and clonal diversity of Staphylococcus aureus in colonization and wound infection with emphasis on diabetic foot infection. Eur J Clin Microbiol Infect Dis 2020; 39: 2235–2246. DOI: 10.1007/s10096-020-03984-8.


1 thought on “LECZENIE RAN 2023; 20 (3)”
Comments are closed.