Artykuł oryginalny | Original paper
Izolaty beztlenowe występujące w zakażonych ranach trudno gojących się oraz ich wrażliwość na leki przeciwbakteryjne
Anaerobic isolates found in infected hard-to-heal wounds and their sensitivity to antimicrobial drugs
Marcin Malka![]() 1, Arkadiusz Krakowiecki
1, Arkadiusz Krakowiecki![]() 1, Magdalena Chojak
1, Magdalena Chojak![]() 1, Marek Pławski
1, Marek Pławski![]() 1, Mariusz Wądołek
1, Mariusz Wądołek![]() 1, Agnieszka Wołowicz
1, Agnieszka Wołowicz![]() 1, Aleksandra Dyczewska
1, Aleksandra Dyczewska![]() 1, Aleksandra Paź
1, Aleksandra Paź![]() 2, Elżbieta Stefaniuk
2, Elżbieta Stefaniuk![]() 3, Tomasz Grzela
3, Tomasz Grzela![]() 4
4
1 Klinika Leczenia Ran PODOS w Warszawie
2 Katedra i Zakład Farmakologii Doświadczalnej i Klinicznej, Warszawski Uniwersytet Medyczny
3 Zakład Mikrobiologii, Wydział Medyczny, Uczelnia Łazarskiego w Warszawie
4 Katedra i Zakład Histologii i Embriologii, Warszawski Uniwersytet Medyczny
Adres do korespondencji: Marcin Malka, Klinika Leczenia Ran PODOS, ul. Ludwika Narbutta 46/48, 02-541 Warszawa, e-mail: marcinmalka@gmail.com
Nadesłano: 3.04.2023
Zaakceptowano: 21.04.2023
Opublikowano: 7.07.2023
LECZENIE RAN 2023; 20 (2): 53–62
Streszczenie
Wstęp: Zauważono, iż obecność beztlenowców jest związana z zakażeniami głębszymi i o cięższym przebiegu. Niewielka liczba doniesień literaturowych sprawia jednak, że infekcje beztlenowe często nie są uwzględniane
w terapii.
Cel pracy: Analiza udziału beztlenowej flory bakteryjnej w etiologii zakażeń ran trudno gojących. Dodatkowo oceniono wrażliwość uzyskanych izolatów na leki przeciwbakteryjne.
Materiał i metody: Analizie poddano 1053 posiewów beztlenowych pobranych od 611 pacjentów w latach 2018–2021. Wszystkie próbki były pobierane z ran z klinicznymi cechami zakażenia metodą biopsji tkankowej. Każdą ranę przygotowywano do posiewu zgodnie z koncepcją „higieny rany”.
Wyniki: Jałowych było 81,7% posiewów, a dodatni wynik posiewu uzyskano w 18,3% próbek. Stwierdzono 229 izolatów beztlenowych (13 rodzajów bakterii), wśród których najliczniej występowały: Bacteroides spp. (47,2%), Peptoniphilus spp. (14,8%), Prevotella spp. (11,8%) i Finegoldia spp. (10,0%). Odsetek izolatów opornych na metronidazol wynosił 2,2%, na amoksycylinę z kwasem klawulanowym 7,0% a na klindamycynę 24,6%. Analizując lekowrażliwość najczęściej izolowanego drobnoustroju beztlenowego – Bacteroides fragilis, stwierdzono 25,4% izolatów opornych na klindamycynę i nie stwierdzono oporności metronidazol.
Wnioski: Flora beztlenowa może być odpowiedzialna za niepowodzenia leczenia przeciwbakteryjnego zakażeń ran trudno gojących się. Uwzględnienie bakterii beztlenowych w procesie diagnostyki i leczenia może istotnie skrócić całkowity czas terapii. W przypadku podejrzenia etiologii beztlenowej w terapii empirycznej najlepszym wyborem wydaje się metronidazol.
Słowa kluczowe: biopsja tkankowa, beztlenowce, zakażenie, rana trudno gojąca się, wrażliwość na antybiotyki.
Abstract
Introduction: It was noted that the presence of anaerobes is associated with deeper and more severe infections. However, due to the small number of literature reports, anaerobic infections are often not considered in therapy.
Aim of the study: To analyze the role of anaerobic bacterial flora in the etiology of hard-to-heal wound infections. In addition, the sensitivity of the obtained isolates to antibacterial drugs was assessed.
Material and methods: 1053 anaerobic cultures taken from 611 patients in 2018-2021 were analyzed. All samples were takenfrom wounds with clinical signs of infection by tissue biopsy. Each wound was prepared for taking cultures in accordance with the concept of “wound hygiene”.
Results: 81.7% of the cultures were sterile and 18.3% of the samples were positive. Two hundred and twenty-nine anaerobic isolates (13 types of bacteria) were found, among which the most numerous were: Bacteroides spp. (47.2%), Peptoniphilus spp. (14.8%), Prevotella spp. (11.8%) and Finegoldia spp. (10.0%). The percentage of isolates resistant to metronidazole was 2.2%, to amoxicillin/clavulanic acid 7.0% and to clindamycin 24.6%. Analyzing drug susceptibility of the most frequently isolated anaerobic microorganism – Bacteroides fragilis, 25.4% of isolates were found resistant to clindamycin and no resistance to metronidazole.
Conclusions: Anaerobic flora may be responsible for the failure of antibacterial treatment of chronic wound infections. Including anaerobic bacteria in the process of diagnosis and treatment can significantly shorten the total treatment time. In the case of suspected anaerobic etiology, metronidazole seems to be the best choice in empirical therapy.
Key words: deep-tissue biopsy, anaerobes, infection, hard-toheal wound, drug sensitivity.
Wprowadzenie
Rany trudno gojące się występują u ok. 6,5 miliona ludzi w USA, a ich leczenie generuje koszty przekraczające 25 miliardów dolarów rocznie [1]. W Polsce brakuje dokładnych danych na temat liczby pacjentów z ranami, szacuje się, iż jest ich ok. 500 tys. [2]. Większość ran zatrzymana jest w fazie zapalnej i nie jest w stanie przejść do fazy proliferacyjnej niezbędnej do zagojenia się rany [3]. Brak postępu w gojeniu ran wiąże się m.in. z niewłaściwym leczeniem zakażenia – zarówno miejscowym, jak i ogólnoustrojowym. Ze względu na doniesienia o narastającej oporności na antybiotyki wśród izolowanych szczepów bakteryjnych, właściwym wydaje się zwrócenie uwagi na kwestie odpowiedniego oczyszczania rany, pobierania materiału do badania mikrobiologicznego, prawidłowych warunków posiewów oraz interpretacji wyniku antybiogramu [4]. Warto tu podkreślić znaczenie techniki pobierania materiału na posiew, zwłaszcza metody biopsji głębokiej jako rekomendowanej w tym zakresie oraz wartości jednoczesnego pobierania kilku posiewów z różnych okolic rany. Wymienione działania stwarzają szansę na wyizolowanie szczepów faktycznie odpowiedzialnych za toczące się zakażenie. Wymazy powierzchowne wydają się mało skuteczną metodą pobierania próbek z zakażonych ran o istotnie mniejszej specyficzności i czułości w porównaniu z badaniami mikrobiologicznymi bioptatów [5].
Bakterie beztlenowe po raz pierwszy zostały omówione jako czynnik etiologiczny zakażenia w zespole stopy cukrzycowej (ZSC) w 1976 r. [6]. Prawie dwie dekady później zauważono, że izolacje beztlenowców w ZSC były związane z głębszymi zakażeniami o cięższym przebiegu oraz właściwym pobieraniem, przechowywaniem i transportem próbek [6].
Zgodnie z aktualnymi wytycznymi Amerykańskiego Towarzystwa Chorób Zakaźnych (Infectious Diseases Society of America, IDSA) w ZSC niedokrwiennej oraz w innych typach ZSC, w których znajdujemy martwicę, obok patogenów tlenowych często występują bakterie beztlenowe koegzystujące w zakażonej ranie [7]. Także w zakażeniach kości obserwuje się szczepy beztlenowe. Niewielka liczba doniesień literaturowych sprawia, że ta przyczyna infekcji często nie jest uwzględniana w terapii [7–9]. Jednak pominięcie tej etiologii może ograniczać skuteczność w kontrolowaniu zakażenia. Na rycinach 1–3 przedstawiono przypadki leczenia ran trudno gojących się, w których obok patogenów tlenowych stwierdzono izolaty beztlenowe.
Cel pracy
Celem pracy była analiza udziału beztlenowej flory bakteryjnej w etiologii zakażeń ran trudno gojących się u pacjentów z Polski leczonych w trybie ambulatoryjnym w ośrodku leczenia ran w latach 2018–2021. Dodatkowo oceniono wrażliwość uzyskanych izolatów na leki przeciwbakteryjne w kontekście ich potencjalnego wykorzystania w terapii empirycznej.
Materiał i metody
Analizie poddano 1053 posiewów beztlenowych pobranych od 611 pacjentów w okresie 9.01.2018–29.06.2021. Wszystkie próbki pobierane były z ran z klinicznymi cechami zakażenia. Zastosowano metodę biopsji tkankowej realizowanej w technice sterylnej (skóra wokół umyta alkoholem, obłożenie sterylnymi serwetami, personel w rękawiczkach sterylnych). Uzyskano 900 bioptatów z tkanek miękkich i 153 z kości.
W tabeli I przedstawiono podział ran i definicje stanowiące podstawę kwalifikacji rany do danej grupy.
Wskazaniem do pobrania materiału do badania mikrobiologicznego zgodnie z zaleceniami IDSA było stwierdzenie co najmniej miejscowych objawów infekcji, takich jak:
- zaczerwienienie,
- nadmierne ucieplenie,
- obrzęk,
- tkliwość lub ból,
- ropny wysięk [7].
Standardową metodą pobierania posiewu była głęboka biopsja tkanek. Każda rana przed pobraniem posiewu przygotowywana była zgodnie z koncepcją „higieny rany” [10]. Wszyscy pracownicy ośrodka przeszli obowiązkowe szkolenie w zakresie stosowania wymienionych standardów. Materiał pobrany na badanie bakteriologiczne był przenoszony na podłoże transportowe typu Amiesa bez węgla [11], a następnie wysyłany do jednego (zawsze tego samego) laboratorium diagnostyki mikrobiologicznej. Do czasu odebrania materiału próbki przechowywane były w temperaturze pokojowej. Stosowane podłoże pozwalało na przechowywanie próbki w takiej temperaturze maks. do 72 godz., jednak zgodnie z rekomendacją producenta dla uzyskania optymalnego wzrostu hodowla powinna być rozpoczęta w ciągu 24 godz. od pobrania materiału [11]. Średni czas przechowywania materiału beztlenowego od pobrania materiału do jego rejestracji zakładzie mikrobiologii w badanej grupie wyniósł 12 godz. i 26 min. Czas ten nie różnił się w grupie posiewów dodatnich (średnio 12 godz. i 23 min) i w grupie posiewów ujemnych (12 godz. i 27 min). Autorzy pracy nie mają wiedzy na temat czasu przechowywania badanych próbek w laboratorium od momentu ich rejestracji do rozpoczęcia badania.
Tabela I. Podział ran i definicje, wg których kwalifikowano ranę do danej grupy
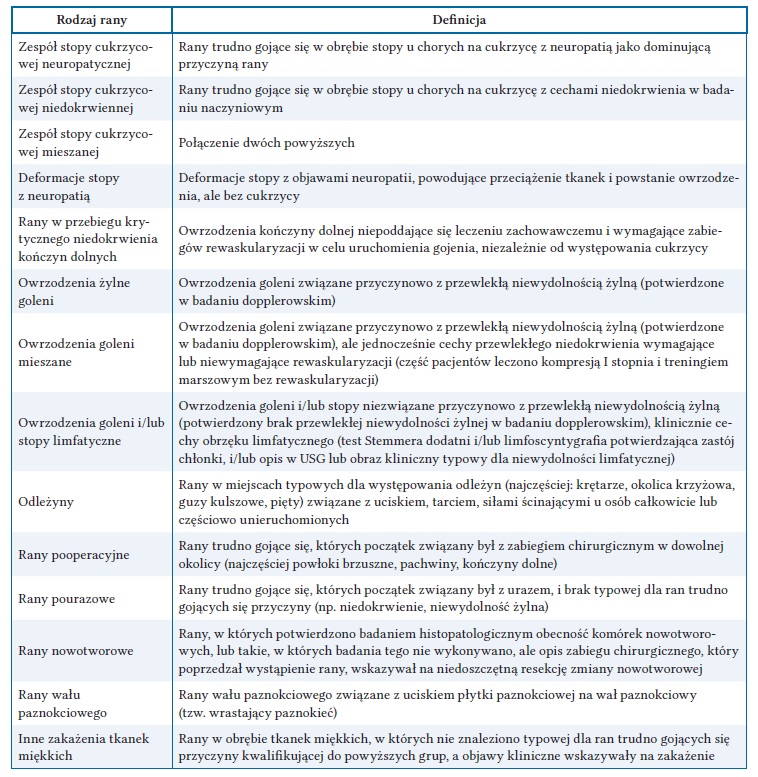
Zarówno posiewy badanych materiałów, jak i identyfikacja oraz oznaczanie i interpretacja lekowrażliwości wyizolowanych szczepów bakteryjnych prowadzone były zgodnie z obowiązującymi rekomendacjami Europejskiego Komitetu ds. Oznaczania Lekowrażliwości Drobnoustrojów (European Committee on Antimicrobial Susceptibility Testing, EUCAST) oraz Krajowego Ośrodka Referencyjnego ds. Oznaczania Lekowrażliwości Drobnoustrojów (KORLD) [12].
Liczbę izolowanych drobnoustrojów beztlenowych przedstawiono w postaci liczby (n) i odsetka (%) wszystkich wyhodowanych szczepów. Obliczenia przeprowadzono przy użyciu oprogramowania statystycznego IBM SPSS Statistics w wersji 26.0. Zmiany w udziale poszczególnych izolatów w perspektywie czasu przedstawiono przy użyciu testu chi-kwadrat dla trendu liniowego.
Wyniki
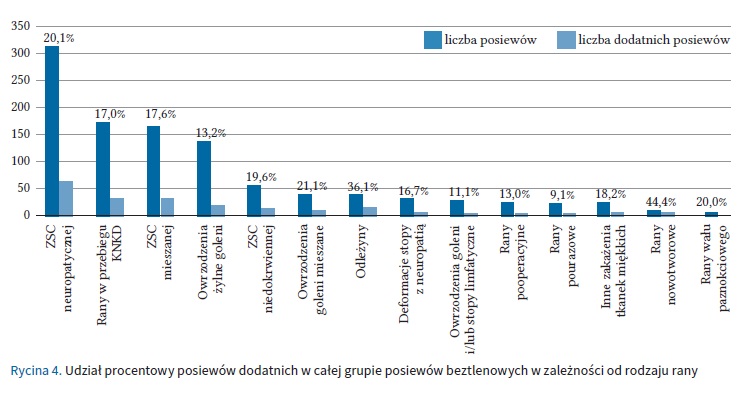
Spośród 1053 próbek materiałów klinicznych pobranych w kierunku flory beztlenowej, 860 (81,7%) posiewów było jałowych, a dodatni wynik posiewu uzyskano w przypadku 193 (18,3%) próbek. Udział posiewów dodatnich w całej grupie posiewów beztlenowych w zależności od rodzaju rany przedstawiono na rycinie 4. Najczęściej izolaty beztlenowe uzyskiwano z ran nowotworowych, a najrzadziej z ran pourazowych. Należy jednak zwrócić uwagę na niewielką liczebność obu grup w przeciwieństwie do materiału uzyskanego od pacjentów z ZSC i krytycznym niedokrwieniem kończyny dolnej (KNKD).
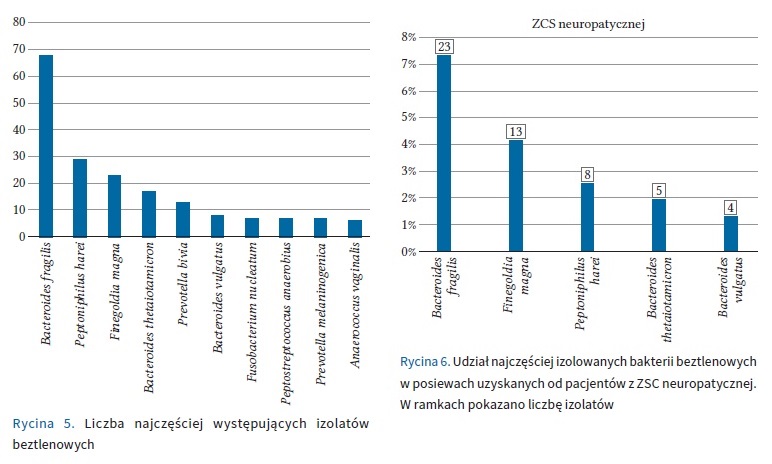
W sumie, w badanych materiałach stwierdzono obecność 229 izolatów beztlenowych. W większości przypadków (n = 160/193; 82,9%) uzyskano wzrost jednego patogenu, w 15,5% próbek (n = 30/193) wyhodowano dwa izolaty, a w 1,6% trzy izolaty (n = 3/193). W żadnej z próbek nie stwierdzono więcej niż 3 patogenów beztlenowych. Jedynie w 4,7% (n = 9/193) przypadkach uzyskano wzrost izolatów beztlenowych przy jednoczesnym wyniku ujemnym w kierunku izolatów tlenowych. W pozostałych przypadkach uzyskano wzrost zarówno izolatów tlenowych, jak i beztlenowych. W badanym materiale wyróżniono 13 rodzajów bakterii beztlenowych, z których najliczniej reprezentowane były: Bacteroides spp. (n = 108; 47,2%), Peptoniphilus spp. (n = 34; 14,8%), Prevotella spp. (n = 27; 11,8%), Finegoldia spp. (n = 23; 10,0%), Fusobacterium spp. (n = 10; 4,4%), Anaerococcus spp. (n = 7; 3,1%), Peptostreptococcus spp. (n = 7; 3,1%). Pojedyncze izolaty należały do rodzajów: Actinomyces spp. (n = 4; 1,7%), Clostridium spp. (n = 3; 1,3%), Propionibacterium spp. (n = 2; 0,9%), Helcococcus spp. (n = 1; 0,4%), Parabacteroides spp. (n = 1; 0,4%), Actinotignum spp. (n = 1; 0,4%) oraz Veillonella spp. (n = 1; 0,4%). Najczęściej izolowano: Bacteroides fragilis (n = 68/229; 29,7%), Peptonihilus harei (n = 29/229; 12,7%) i Finegoldia magna (n = 23/229, 10,0%).
Na rycinie 5 przedstawiono 10 najczęściej izolowanych bakterii beztlenowych.

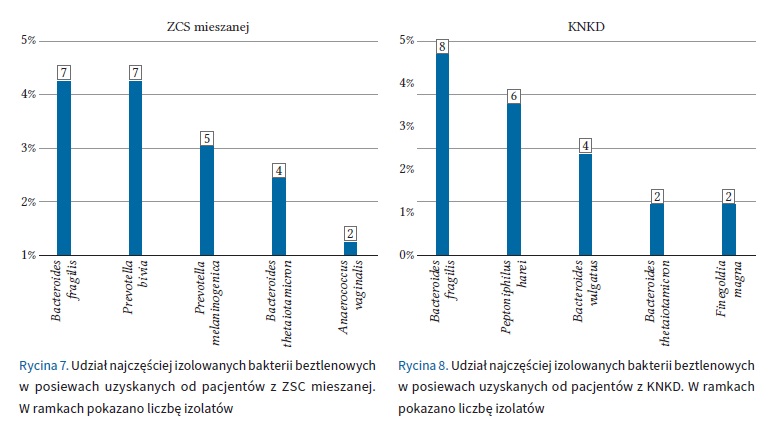
Liczba posiewów pobieranych w kierunku bakterii beztlenowych, w kolejnych latach obserwacji, istotnie wzrastała od 11,8% w 2018 r. do 41,7% wszystkich posiewów bakteryjnych w 2021 r. (p < 0,001). Nie stwierdzono istotnych zmian w zakresie częstości występowania najczęstszych izolatów beztlenowych na przestrzeni lat. Jedynie w przypadku Prevotella bivia zaobserwowano znamienną tendencję wzrostową. Na rycinie 8 przedstawiono udział procentowy pięciu najczęściej stwierdzanych izolatów w etiologii zakażeń beztlenowych na przestrzeni lat 2018–2021.
Z tkanek miękkich bakterie beztlenowe wyizolowano w 19,4% przypadków, z czego 51,1% stanowiły próbki z ran w przebiegu ZSC (wszystkich typów). W materiale pochodzącym z kości bakterie beztlenowe stwierdzono w 15,0% przypadków, z czego 69,6% próbek uzyskano z ran w przebiegu ZSC (wszystkich typów). Bakterie beztlenowe izolowano najczęściej z tkanek miękkich i z kości pochodzących z ran od pacjentów z ZSC neuropatycznej.
Biorąc pod uwagę wszystkie wyizolowane bakterie beztlenowe odsetek szczepów opornych na klindamycynę wynosił 24,6%, na amoksycylinę z kwasem klawulanowym 7,0%, a na metronidazol 2,2%. Nie stwierdzono oporności na karbapenemy. Odsetek szczepów opornych na penicylinę, amoksycylinę lub piperacylinę przekraczał 60%.
Na rycinie 9 przedstawiono odsetek izolatów beztlenowych opornych na poszczególne leki przeciwbakteryjne.
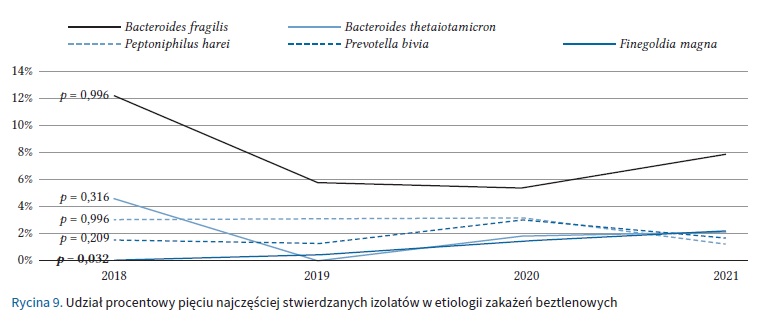
Analizując lekowrażliwość najczęściej izolowanego drobnoustroju beztlenowego – Bacteroides fragilis, stwierdzono 25,4% izolatów opornych na klindamycynę. Drobnoustrój ten jest naturalnie oporny na penicylinę i amoksycylinę. Nie stwierdzono oporności na karbapenemy i metronidazol. Odsetek izolatów Bacteroides fragilis opornych na wybrane antybiotyki przedstawiono na rycinie 10.
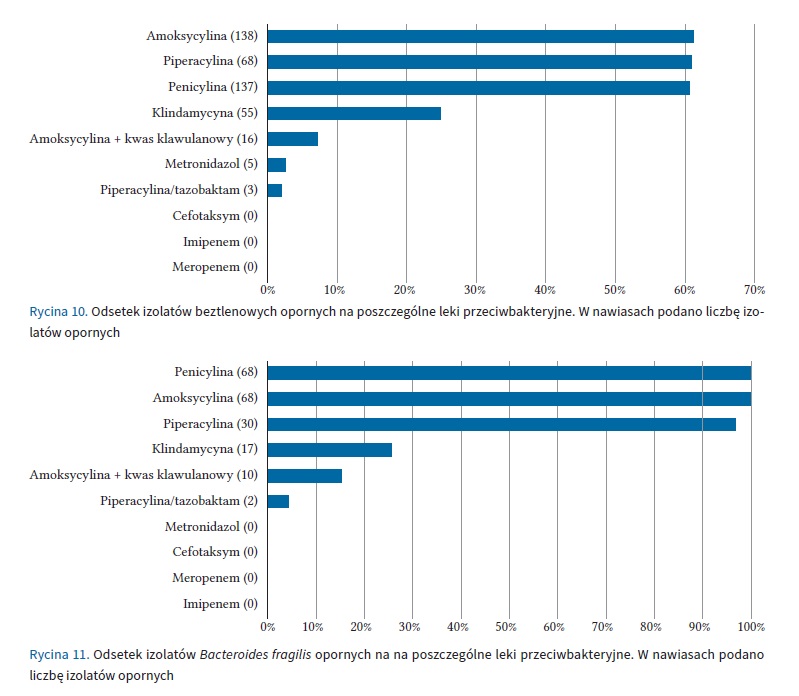
Dla trzech najczęściej izolowanych beztlenowców (Bacteroides fragilis, Peptoniphilus harei, Finegoldia magna) przeanalizowano oporność na leki przeciwbakteryjne w analizowanym okresie. W odniesieniu do wyżej wymienionych drobnoustrojów nie stwierdzono istotnych statystycznie zmian w oporności na następujące leki: metronidazol, klindamycynę, penicylinę, amoksycylinę, amoksycylinę z kwasem klawulanowym, piperacylinę z tazobaktamem, cefotaksym, imipenem i meropenem.
Dyskusja
Wiele danych wskazuje na to, że za zakażenie ran trudno gojących się odpowiada często kilka bakterii jednocześnie. Podejmując decyzje diagnostyczne i terapeutyczne, ważne jest, aby uwzględniać polikulturowość mikrobioty ran przewlekłych [13]. Beztlenowce zwykle występują z bakteriami tlenowymi, rzadko są to monokultury [14]. W badaniu 80 pacjentów ze stopą cukrzycową, przeprowadzonym przez Gadepalli i wsp. zakażenie spowodowane przez beztlenowce stwierdzono w 1 przypadku [15]. Z kolei zakażenia o etiologii tlenowo-beztlenowej występowały w 33,8% [15]. W badaniu Citrona i wsp. 49,3% izolatów należało do grupy bakterii beztlenowych, w tym jedynie 1,3% to monokultury [16]. W materiale autorów niniejszej pracy monokultury beztlenowe stanowiły 4,7% (9/193). Powyższe obserwacje wskazują na konieczność jednoczesnego pobierania materiału mikrobiologicznego w kierunku bakterii tlenowych i beztlenowych.
W prezentowanym materiale, w grupie posiewów wykonywanych w kierunku bakterii beztlenowych brak wzrostu stwierdzono aż w 81,67% (n = 860) badań. Oczywiście, może być to wynik niewielkiego udziału flory beztlenowej w etiologii zarejestrowanych zakażeń, jednak nie można wykluczyć wpływu zastosowania nieoptymalnych podłoży transportowych w obsługującej ośrodek pracowni mikrobiologicznej i zbyt długiego przechowywania próbek do czasu rozpoczęcia inkubacji. Rutynowe zastosowanie specjalistycznych próbówek (np. Venturi Transystem®) lub płynnych podłoży transportowych (np. eSwab®) może zwiększyć wykrywalność gatunków beztlenowych odpowiedzialnych za zakażenia ran trudno gojących się [17–20]. Kolejnym istotnym parametrem wpływającym na wynik posiewu beztlenowego jest czas przechowywania próbki przed rozpoczęciem hodowli. Niewątpliwie konieczne jest skrócenie czasu transportu próbki do laboratorium do 24 godz. [11]. Rekomenduje się nawet, aby czas od pobrania do rozpoczęcia inkubacji mieścił się w zakresie 3–6 godz. [21]. Zmiana podłoży stosowanych w posiewach beztlenowych i skrócenie czasu transportu próbki do laboratorium wymaga zmian schematów postępowania w ośrodkach zajmujących się leczeniem ran i medycznych laboratoriach mikrobiologicznych, do których próbki są kierowane. Takie działania wydają się jednak nieuniknione w celu zwiększenia wykrywalności szczepów beztlenowych.
Średni udział patogenów beztlenowych w 44 badaniach przeanalizowanych przez Charlesa i wsp. (13 012 pacjentów) wyniósł 11% [22]. W prezentowanym materiale dodatnie hodowle w kierunku beztlenowców uzyskano w przypadku 18,3% (n = 193) posiewów. Dotyczyły one odpowiednio 31,6% próbek pochodzących z odleżyn, 18,9% próbek z ran w przebiegu zespołu stopy cukrzycowej (łącznie wszystkich typów), 17,0% próbek z ran w przebiegu KNKD i tylko 13,2% próbek pochodzących z owrzodzeń żylnych goleni. Trengove i wsp. wykryli beztlenowce w jednej czwartej próbek pochodzących zarówno z zakażonych, jak i niezakażonych owrzodzeń żylnych goleni [23]. W obserwacjach MacDonalda i wsp. bakterie beztlenowe stanowiły 6% izolatów z zakażonych ran w przebiegu ZSC [24]. W pracy zespołu Rondasa i wsp. bakterie beztlenowe wyizolowano tylko z 2% ran przewlekłych [25]. W powyższym kontekście ciekawą obserwację poczynili Bowler i Davies, wykazując obecność beztlenowców aż w 82% zakażonych owrzodzeń goleni [26]. Trzeba jednak zwrócić uwagę, iż badanie to pochodzi z 1999 r., kiedy obowiązywały inne standardy przygotowania rany do pobrania materiału oraz samego badania
mikrobiologicznego. Rany uwzględnione w tym badaniu przed pobraniem posiewu były jedynie przemywane solą fizjologiczną, a same posiewy były pobierane techniką zbliżoną do techniki Levina, także z tkanki martwiczej. Wyniki cytowanego badania znacznie odbiegają od wyników prezentowanych przez innych autorów. Przyczyną tak dużej rozbieżności wyników może być izolowanie drobnoustrojów kolonizujących ranę, a nie faktycznie odpowiedzialnych za zakażenie.
Bakterie beztlenowe mogą odgrywać równie istotną rolę w zapaleniu kości i szpiku, zwłaszcza w ZSC, jak bakterie tlenowe [9]. Dane z prezentowanego w niniejszej pracy badania wskazują, że wyskrobiny z kości nie powinny być pomijane w poszukiwaniu beztlenowców jako czynnika etiologicznego zapalenia kości i szpiku. W bieżącym materiale, w przypadku próbek pochodzących z kości bakterie beztlenowe izolowano w 15,0%, z czego 69,6% próbek pochodziła z ran w przebiegu ZSC (wszystkich typów). W badaniu van Astena i wsp. [9] bakterie beztlenowe wykryto w 23,1% próbek pochodzących z kości od pacjentów z ZSC. W badaniach Senneville’a i wsp. [27] oraz Ertugrula i wsp. [28] tylko u 3%
i 5% pacjentów.
W ciągu ostatnich dziesięcioleci wrażliwość bakterii beztlenowych na antybiotyki uległa znaczącej zmianie [29]. Celowana terapia przeciwbakteryjna oparta na aktualnym antybiogramie zwiększa istotnie szanse na osiągnięcie sukcesu klinicznego. Jednak leczenie przeciwbakteryjne zwykle jest rozpoczynane bez dokładnej znajomości czynnika etiologicznego. Znajomość trendów wrażliwości pozwala na właściwy dobór leków przeciwbakteryjnych do terapii empirycznej. Wyniki badania lekowrażliwości izolatów z prezentowanego materiału wskazują, że tylko 2,2% bakterii beztlenowych pozostaje opornych na metronidazol. W odniesieniu do najczęściej występującego Bacteroides fragilis nie stwierdzono ani jednego izolatu opornego na ten chemioterapeutyk. Oporność bakterii beztlenowych na amoksycylinę z kwasem klawulanowym w prezentowanym materiale wynosiła 7,0%, a dla izolatów Bacteroides fragilis – 14,7%.
Dane z piśmiennictwa wskazują na wzrost oporności izolatów Bacteroides fragilis na leki przeciwbakteryjne, w tym na amoksycylinę z kwasem klawulanowym [31–32]. Z kolei Pitocco i wsp. zaobserwowali 21,4% izolatów Bacteroides fragilis opornych na piperacylinę, nie stwierdzili jednak oporności na amoksycylinę z kwasem klawulanowym, imipenem lub meropenem [33].
Niepokojącym zjawiskiem jest wzrost oporności na antybiotyki także innych gatunków Bacteroides spp. [34]. Fakt ten wskazuje na konieczność identyfikacji do poziomu gatunku wszystkich izolowanych potencjalnych patogenów. Potwierdzenie stanowią wyniki niniejszej pracy, w której wśród 108 izolatów rodzaju Bacteroides spp. 37,0% (n = 40) należało do innych gatunków niż Bacteroides fragilis, a 15,7% stanowił Bacteroides thetaiotaomicron (n = 17). Boyanova i wsp. w swojej pracy dotyczącej lekowrażliwości szczepów Bacteroides spp. i Parabacteroides spp. opisują 7,8-krotny wzrost oporności na amoksycylinę z kwasem klawulanowym w ciągu 19 lat w Kanadzie i 10,4-krotny w ciągu 20 lat w Europie [29]. Obserwacje te dotyczą materiału pochodzącego z zakażeń o różnej lokalizacji. W materiale uzyskanym jedynie z zakażonych ran trudno gojących się w latach 2018–2021 nie stwierdzono narastania oporności wśród trzech najczęściej występujących izolatów, w odniesieniu do następujących leków: metronidazol, klindamycyna, penicylina, amoksycylina, amoksycylina z kwasem klawulanowym, piperacylina z tazobaktamem, cefotaksym, imipenem i meropenem.
Wnioski
Pominięcie udziału flory beztlenowej w etiologii zakażeń ran trudno gojących się może być przyczyną niepowodzenia leczenia przeciwbakteryjnego. Właś-
ciwe rozpoznanie i skuteczne leczenie (miejscowe, a w wybranych przypadkach ogólnoustrojowe) skraca fazę zapalną, a co za tym idzie – całkowity czas leczenia. Zasadne wydaje się dalsze monitorowanie mikrobioty beztlenowej pod względem jakościowym, a także w kontekście oporności na leki przeciwbakteryjne.
Oświadczenie
Autorzy deklarują brak konfliktu interesów.
Piśmiennictwo
- Sen CK, Gordillo GM, Roy S i wsp. Human skin wounds: a major and snowballing threat to public health and the economy. Wound Repair Regen 2009; 17: 763–771. DOI: 10.1111/j.1524-475X.2009.00543.x.
- Sopata M, Jawień A, Mrozikiewicz-Rakowska B i wsp. Wytyczne postępowania miejscowego w ranach niezakażonych, zagrożonych infekcją oraz zakażonych – przegląd dostępnych substancji przeciwdrobnoustrojowych stosowanych w leczeniu ran. Zalecenia Polskiego Towarzystwa Leczenia Ran. Leczenie Ran 2020; 17: 1–21. DOI: https://doi.org/10.5114/lr.2020.96820.
- Li J, Chen J, Kirsner R. Pathophysiology of acute wound healing. Clin Dermatol 2007; 25: 9–18. DOI: 10.1016/j.clindermatol.2006.09.007
- Nagy E, Boyanova L, Justesen US; ESCMID Study Group of Anaerobic Infections. How to isolate, identify and determine antimicrobial susceptibility of anaerobic bacteria in routine laboratories. Clin Microbiol Infect 2018; 24: 1139–1148. DOI: 10.1016/j.cmi.
2018.02.008. - Chakraborti C, Le C, Yanofsky A. Sensitivity of superficial cultures in lower extremity wounds. J Hosp Med 2010; 5: 415–420. DOI: 10.1002/jhm.688.
- Louie TJ, Bartlett JG, Tally FP, Gorbach SL. Aerobic and anaerobic bacteria in diabetic foot ulcers. Ann Intern Med 1976; 85: 461–463. DOI: 10.7326/0003-4819-85-4-461.
- Lipsky BA, Berendt AR, Cornia PB i wsp. 2012 Infectious Diseases Society of America clinical practice guideline for the diagnosis and treatment of diabetic foot infections. Clin Infect Dis 2012; 54: e132–e173. DOI: 10.1093/cid/cis346.
- Gerding DN. Foot infections in diabetic patients: the role of anaerobes. Clin Infect Dis 1995; 20 Suppl 2: S283–S288. DOI: 10.1093/clinids/20.supplement_2.s283.
- van Asten SA, La Fontaine J, Peters EJ i wsp. The microbiome of diabetic foot osteomyelitis. Eur J Clin Microbiol Infect Dis 2016; 35: 293–298. DOI: 10.1007/s10096-015-2544-1.
- Murphy C, Atkin L, Dissemond J i wsp. Defying hard-to-heal wounds with an early antibiofilm intervention strategy: ‘wound hygiene’. J Wound Care 2019; 28: 818–822. DOI: 10.12968/jowc.2019.28.12.818.
- Amies – Agar Swabs – Deltalab. (n.d.). Retrieved January 12, 2023.Dostępne na: https://www.deltalab.es/en/producto/amies-sterile/.
- Hryniewicz W, Żabicka D. Stanowisko Zespołu Roboczego ds. oznaczania lekowrażliwości zgodnie z zaleceniami EUCAST w sprawie najczęściej zgłaszanych pytań dotyczących stosowania rekomendacji EUCAST wersja 5.0 15 grudnia 2021. Dostępne na: https://www.korld.nil.gov.pl.
- Dowd SE, Sun Y, Secor PR i wsp. Survey of bacterial diversity in chronic wounds using pyrosequencing, DGGE, and full ribosome shotgun sequencing. BMC Microbiol 2008; 8: 43. DOI: 10.1186/1471-2180-8-43.
- Choi Y, Banerjee A, McNish S i wsp. Co-occurrence of Anaerobes in Human Chronic Wounds. Microb Ecol 2019; 77: 808–820. DOI: 10.1007/s00248-018-1231-z.
- Gadepalli R, Dhawan B, Sreenivas V i wsp. A clinico-microbiological study of diabetic foot ulcers in an Indian tertiary care hospital. Diabetes Care 2006; 29: 1727–1732. DOI: 10.2337/dc06-0116.
- Citron DM, Goldstein EJ, Merriam CV i wsp. Bacteriology of moderate-to-severe diabetic foot infections and in vitro activity of antimicrobial agents. J Clin Microbiol 2007; 45: 2819–2828. DOI: 10.1128/JCM.00551-07.
- Hudspeth MK, Citron DM, Goldstein EJ. Evaluation of a novel specimen transport system (Venturi Transystem) for anaerobic bacteria. Clin Infect Dis 1997; 25 Suppl 2: S132–S133. DOI:
10.1086/516198. - Van Horn KG, Audette CD, Sebeck D, Tucker KA. Comparison of the Copan ESwab system with two Amies agar swab transport systems for maintenance of microorganism viability. J Clin Microbiol 2008; 46: 1655–1658. DOI: 10.1128/JCM.02047-07
- Demuyser T, De Geyter D, Van Dorpe D i wsp. Extensive evaluation of fastidious anaerobic bacteria recovery from the Copan eSwab® transport system. J Microbiol Methods 2018; 144: 73–78. DOI: 10.1016/j.mimet.2017.11.009.
- Tyrrell KL, Citron DM, Leoncio ES, Goldstein EJ. Comparison of the Copan eSwab System with an Agar Swab Transport System for Maintenance of Fastidious Anaerobic Bacterium Viability. J Clin Microbiol 2016; 54: 1364–1367. DOI: 10.1128/
JCM.03246-15. - Chapter 1-2. Anaerobic infections (general): testing anaerobic infections. (n.d.). Dostępne na: https://doi.org/10.1007/s10156-010-0132-y.
- Charles PG, Uçkay I, Kressmann B i wsp. The role of anaerobes in diabetic foot infections. Anaerobe 2015; 34: 8–13. DOI: 10.1016/
j.anaerobe.2015.03.009. - Trengove NJ, Stacey MC, McGechie DF, Mata S. Qualitative bacteriology and leg ulcer healing. J Wound Care 1996; 5: 277–280. DOI: 10.12968/jowc.1996.5.6.277.
- Ge Y, MacDonald D, Hait H i wsp. Microbiological profile of infected diabetic foot ulcers. Diabet Med 2002; 19: 1032–1034. DOI: 10.1046/j.1464-5491.2002.00696_1.x.
- Rondas AA, Schols JM, Halfens RJ, Stobberingh EE. Swab versus biopsy for the diagnosis of chronic infected wounds. Adv Skin Wound Care 2013; 26: 211–219. DOI: 10.1097/01.ASW.0000428984.58483.aa
- Bowler PG, Davies BJ. The microbiology of infected and noninfected leg ulcers. Int J Dermatol 1999; 38: 573–578. DOI: 10.1046/j.1365-4362.1999.00738.x.
- Senneville E, Melliez H, Beltrand E i wsp. Culture of percutaneous bone biopsy specimens for diagnosis of diabetic foot osteomyelitis: concordance with ulcer swab cultures. Clin Infect Dis 2006; 42: 57–62. DOI: 10.1086/498112.
- Ertugrul MB, Baktiroglu S, Salman S i wsp. The diagnosis of osteomyelitis of the foot in diabetes: microbiological examination vs. magnetic resonance imaging and labelled leucocyte scanning. Diabet Med 2006; 23: 649–653. DOI: 10.1111/j.1464-5491.2006.01887.x.
- Boyanova L, Kolarov R, Mitov I. Recent evolution of antibiotic resistance in the anaerobes as compared to previous decades. Anaerobe 2015; 31: 4–10. DOI: 10.1016/j.anaerobe.2014.05.004
- Brook I. Treatment of anaerobic infection. Expert Rev Anti Infect Ther 2007; 5: 991–1006. DOI: 10.1586/14787210.5.6.991.
- Jamal W, Shahin M, Rotimi VO. Surveillance and trends of antimicrobial resistance among clinical isolates of anaerobes in Kuwait hospitals from 2002 to 2007. Anaerobe 2010; 16: 1–5. DOI: 10.1016/
j.anaerobe.2009.04.004 - Nagy E, Urbán E, Nord CE; ESCMID Study Group on Antimicrobial Resistance in Anaerobic Bacteria. Antimicrobial susceptibility of Bacteroides fragilis group isolates in Europe: 20 years of experience. Clin Microbiol Infect 2011; 17: 371–379. DOI: 10.1111/j.1469-0691.2010.03256.x.
- Pitocco D, Spanu T, Di Leo M i wsp. Diabetic foot infections: a comprehensive overview. Eur Rev Med Pharmacol Sci 2019; 23 (2 Suppl): 26–37. DOI: 10.26355/eurrev_201904_17471.
- Snydman DR, Jacobus NV, McDermott LA i wsp. Lessons learned from the anaerobe survey: historical perspective and review of the most recent data (2005-2007). Clin Infect Dis 2010; 50 Suppl 1: S26–S33. DOI: 10.1086/647940.

